牛膝配方颗粒
本品为苋科植物牛膝 Achyranthes bidentata Bl.的干燥根经炮制并按标准汤剂的主要质量指标加工制成的配方颗粒。
2021年4月29日,国家药典委员会发布《关于执行中药配方颗粒国家药品标准有关事项的通知》:经国家药品监督管理局批准,首批160个中药配方颗粒国家药品标准已正式颁布,将于2021年11月1日正式实施。
迪马科技依据国家药品标准YBZ-PFKL-2021098,重现了牛膝配方颗粒的检测方案,可供大家参考。
一、特征图谱
1.样品制备
参照物溶液 取牛膝对照药材1.0g,加水20mL,煮沸30分钟,过滤,滤液蒸干,加水10mL,超声处理20分钟,放冷,摇匀,滤过,取续滤液,作为对照药材参照物溶液。另取β-蜕皮甾酮对照品适量,精密称定,加甲醇制成每1mL含25μg的溶液,作为对照品参照物溶液。
供试品溶液 取本品适量,研细,取约0.2 g,精密称定,置具塞锥形瓶中,精密加入水10mL,称定重量,超声处理20分钟,放冷,再称定重量,用水补足减失的重量,摇匀,滤过,取续滤液,即得。
2.分析条件
色谱柱:Navigatorsil C18,2.1mm×100mm,2.7μm(Cat#88003)
流动相:A-乙腈 B-0.05%甲酸溶液
流速:0.3mL/min
进样量:1μL
柱温:40℃
检测波长:270nm

3.实验图谱
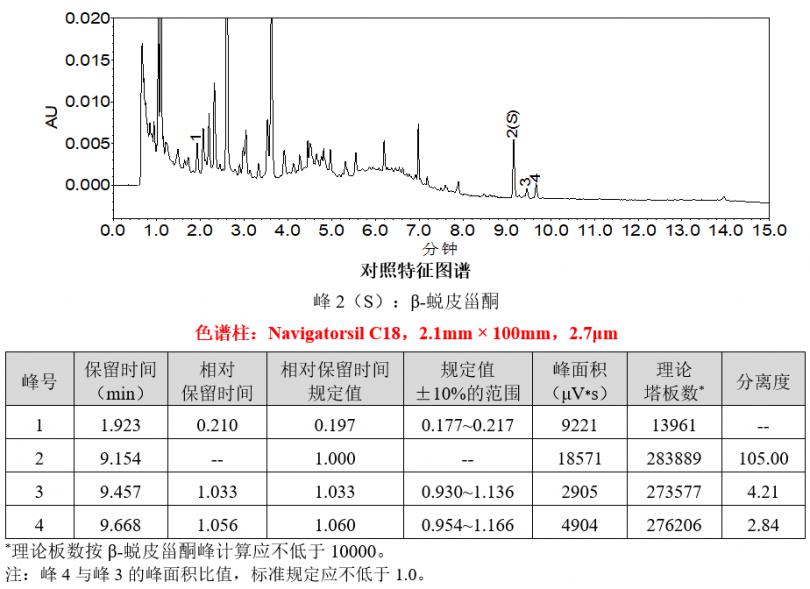
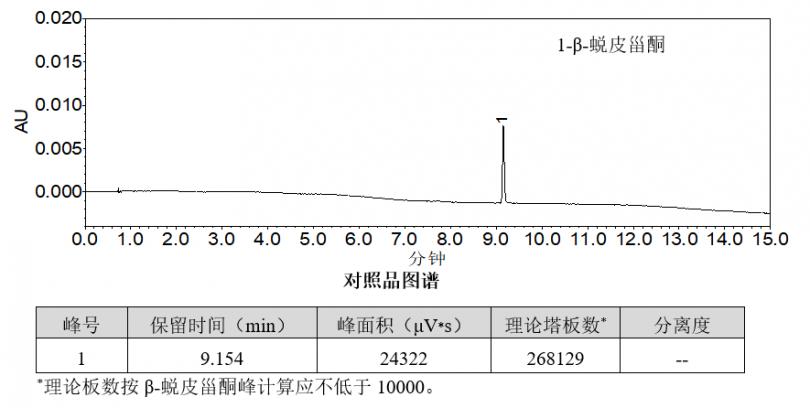
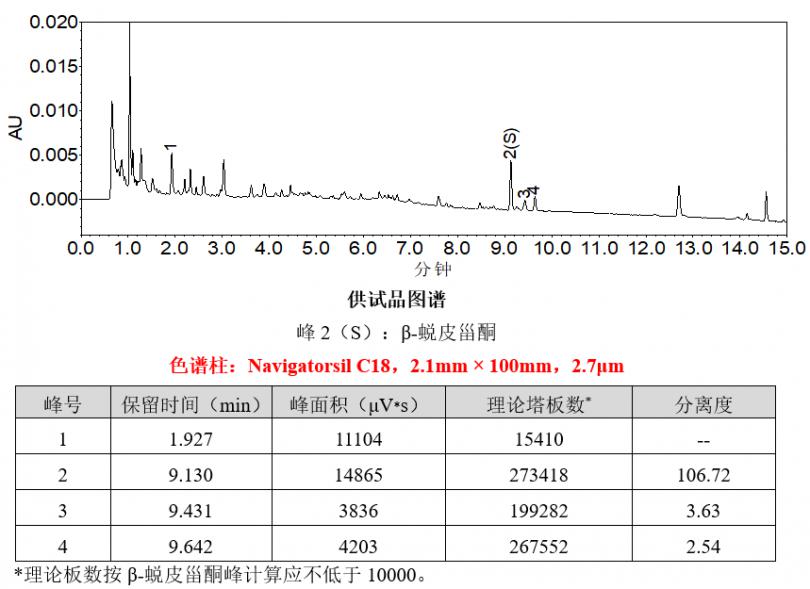
4.实验结果
使用色谱柱Navigatorsil C18,2.1mm×100mm,2.7μm(Cat#88003)检测牛膝配方颗粒,供试品色谱中呈现4个特征峰,并与对照药材参照物色谱中的4个特征峰保留时间相对应;计算各特征峰与S峰(β-蜕皮甾酮峰)的相对保留时间分别为0.210(峰1)、1.033(峰3)、1.056(峰4),均在规定值±10%范围内;计算峰4与峰3的相对峰面积为1.7,符合方法要求。
二、含量测定
1.样品制备
对照品溶液 取β-蜕皮甾酮对照品适量,精密称定,加甲醇制成每1mL含10μg的溶液,即得。
供试品溶液 取本品适量,研细,取约0.2g,精密称定,置具塞锥形瓶中,精密加入水10mL,称定重量,超声处理20分钟,放冷,再称定重量,用水补足减失的重量,摇匀,滤过,取续滤液,即得。
2.分析条件
色谱柱:Endeavorsil C18,2.1mm×100mm,1.8μm(Cat#87003)
流动相:乙腈-水-甲酸(16︰84︰0.1)
流速:0.3mL/min
进样量:1μL
柱温:35℃
检测波长:250nm
3.实验图谱
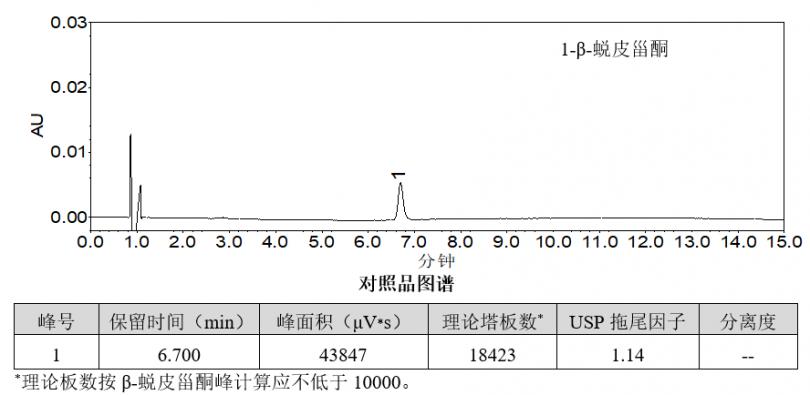
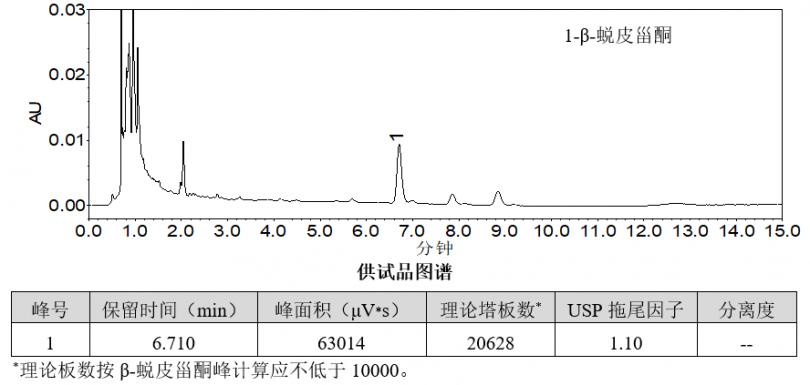
4.实验结果
经测定本品每1g含β-蜕皮甾酮(C27H44O7)的含量为0.72mg,在方法规定的范围内(0.39mg~1.17mg)。
中药配方颗粒是近几年发展较快的中药制剂,由单味中药饮片经提取浓缩而成,供中医临床配方用,具有见效快,吸收好,
请问:中药配方申请国家食品药品监督管理局批准文号的程序?大概需要多长时间?谢谢!从开始申请到拿到批准生产文
近日,经国家药品监督管理局批准相继发布了196个中药配方颗粒国家标准,这些标准充分体现了中药质量的控制特点和
自 2021 年 2 月,国家药典委宣布《关于结束中药配方颗粒试点工作的公告》后结束试点工作以来,陆续颁布了四批国家
国务院联防联控机制综合组12月7日发布“新十条”基于对疾病病原体的认识、人群免疫水平和社会公共卫生系统的判断
为了规范中药配方颗粒的生产,保证临床liaoxiao,国家药典委及各省药监局一直在陆续发布中药配方颗粒guo
中药配方颗粒有效期为三年。药品稳定性有物理稳定性、微生物稳定性和化学稳定性三个方面。物理稳定性是指药品因物理
如题,如果知道什么偏方或者其他药物ZL方法也可以,不胜感激! 结核性胸膜炎 胸膜炎是胸膜的炎症,可由
纳米技术是一个快速发展的新兴领域,其发展和前景也给科学家和工程师们带来了
距离国家药典委员会公示DY批160种中药配方颗粒统一标准刚满一年,如何通过科学、合理的质量控制来规范中药配方