- 为您推荐:
 钠
钠
 仪器网
钠
仪器网
钠
钠(na),英文为Sodium,元素符号为Na,原子序数为11,相对原子质量为22.989768,是最常见的碱金属元素。钠是一种带有银白色光泽的软金属,质软,容易切割。金属钠主要用于制造车用汽油的抗暴剂,还用于制取钛,及生产氢氧化钠、氨基钠、氰化钠等。钠的化合物可以应用在生活、医药、农业和摄影器材中,如氯化钠就是我们日常生活中用到的食盐。
钠的由来
钠,元素符号为Na,来自于拉丁文“natrium”。1807年,化学家戴维用电解熔融的氢氧化钠的方法制得钠。钠元素在地壳中含量第七(O、Si、Al、Fe、Ca、Mg、Na...)。钠可以通过电解熔融的氯化钠(食盐),硼砂或冰晶石获得。
钠的物理性质
钠是一种柔软、银白色、有光泽的金属。它的密度比水小,比煤油的密度大,能浮在水面上。熔点97.81°C,沸点882.9°C,能导电导热。相对原子质量:22.99,原子体积为23.7立方厘米/摩尔。
钠的化学性质
钠具有很强的还原性,是一种活泼的金属元素。
(1)钠容易与非金属反应
金属钠放置在空气中,会迅速被氧化而生成氧化钠;
4Na+O2=2Na2O
钠在空气(或氧气)中燃烧生成过氧化钠。
2Na+O2=燃烧=Na2O2(黄色火焰),
钠在氯气燃烧,生成氯化钠。
2Na+Cl2=点燃=NaCl(白烟)
(2)钠与水反应
钠跟水反应,并放出热量,发出嘶嘶响声,产生气体。
2Na+2H2O =2NaOH +H2↑
(3)钠与酸反应
钠跟硫化合反应时,容易发生爆炸。
2Na+S=Na2S(硫化钠)
钠的化合物
钠的化合物主要有氧化钠、过氧化钠、碳酸钠、碳酸氢钠等。
氧化钠(Na2O),白色固体,不稳定,容易与水发生反应生成氢氧化钠。
过氧化钠(Na2O2),淡黄色粉末,溶于水,具有强氧化性、漂白性等。
钠的存放
由于金属钠的化学性质非常活泼,易与空气中的O2、H2O等反应,所以少量金属钠可保存在煤油里,大量的金属钠则存在铁筒中用石蜡密封。取用时一般先用镊子把钠从煤油中夹出来,并用滤纸把表面的煤油吸干,然后再做有关实验。
钠的用途
自然界中钠只能以化合态的形态存在,主要以氯化钠的形式存在。钠是一种强还原剂,工业上用它还原金属钛、锆、铌等;另外钠和钾的合金在常温下呈液态,是原子反应堆的导热剂;钠也可用于制高压钠灯。
钠的两种化合物-氧化钠和过氧化钠,他们之间的区别有哪些呢?氧化钠,化学式为Na2O,白色粉末状固体,是碱性氧化物,具有腐蚀性、强刺激性,可致人体灼伤。人接触后可... [查看全部]
钠是一种金属元素,呈银白色,质软,容易切割。金属钠是最 早利用电解氢氧化钠的方法制得,现在工业上多数用电解氯化钠的方法制得。金属钠用于制备氰 化 钠、过氧化钠、染料中间体、医药中间体、海绵钛等,以及多种化学药物或作还原剂。
金属钠的制备
电解氯化钠制金属钠通常在电解槽里进行。电解时氯化钠需要熔融,用熔融温度约为580℃的质量分数为40%氯化钠和60%氯化钙的低温共熔物(即两种或两种以上物质形成的熔点最低的混合物),降低了电解时所需的温度,从而也减低了钠的蒸气压。电解时,氯气在阳极放出,当电流通过熔盐时,金属钠和金属钙同时被还原出来,浮在阴极上方的熔盐上面,从管道溢出。把熔融的金属混合物冷却到105~110℃,金属钙成晶体析出,经过滤就可以把金属钠跟金属钙分离。
金属钠的危害
金属钠对人体的危害
金属钠为碱金属,能腐蚀人体,在空气中易氧化自燃,燃烧产生的烟(主要含氧化钠)对鼻、喉及上呼吸道有腐蚀作用及极强的刺激作用。同时,金属钠有极强的腐蚀性,可造成化学性烧伤或热灼伤。眼睛接触会造成严重的眼睛烧伤。
金属钠对环境的危害
金属钠本身对环境无危害,但燃烧时,产生烟尘,对周围环境造成危害。如金属钠与空气直接接触,与空气中的氧和水发生反应,遇水发生剧烈反应,生成氢氧化钠和氢气,发生燃烧或爆炸。金属钠在氯、氟中能剧烈燃烧,燃烧时火焰呈黄色,与酸作用生成相应的盐类和氢气,同时能立即燃烧爆炸。能与氧化剂发生剧烈反应,具有强腐蚀性、强刺激性。
金属钠的保存
实验室把金属钠通常保存在液体石蜡中。瓶子要密封,在阴凉处保存。工业上把金属钠用煤油或柴油封装到金属桶中。
金属钠着火处理
金属钠一旦着火,可以用干燥的苏打灰、氯化钠(干燥粉末)、干沙土进行覆盖或用碱金属灭火器灭火,然后铲入干燥金属容器中,再用干燥的苏打灰、氯化钠(干燥粉末)、干沙土进行覆盖。
注意事项:不能用水,二氧化碳、泡沫、碳酸氢钠、碳酸氢钾作为灭火剂。
... 查看全文钠的两种化合物-氧化钠和过氧化钠,他们之间的区别有哪些呢?
氧化钠,化学式为Na2O,白色粉末状固体,是碱性氧化物,具有腐蚀性、强刺激性,可致人体灼伤。人接触后可引起灼伤、头痛、恶心、呕吐、咳嗽、喉炎、气短。
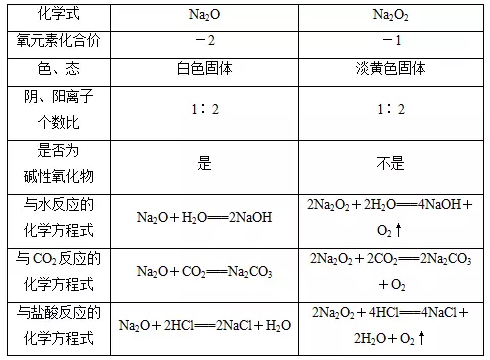
氧化钠是碱性氧化物,其中氧元素为-2价,钠元素为+1价,氧化钠遇水起剧烈化合反应,形成氢氧化钠。氧化钠与二氧化碳反应生成碳酸钠,与盐酸反应生成氯化钠和水。
过氧化钠,化学式为Na2O2,淡黄色的粉末状固体。过氧化钠易潮解、有腐蚀性,应密封保存。过氧化钠具有强氧化性,在熔融状态时遇到棉花、炭粉、铝粉等还原性物质会发生爆炸。因此存放时应注意安全,不能与易燃物接触。
过氧化钠不属于碱性化合物,其中氧元素显-1价,钠元素显+1价,可以把过氧化钠溶解在低温的硫酸中,然后减压蒸馏即可得到过氧化氢(H2O2),过氧化氢会分解成水和氧气。过氧化钠可与水、酸反应,生成氢氧化钠和过氧化氢。过氧化钠还能氧化一些金属。
过氧化钠还可以用于消毒、杀菌和漂白等,在工业上常用做漂白剂、杀菌剂、消毒剂、去臭剂、氧化剂等。
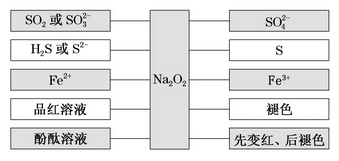
过氧化钠的强氧化性:
1、从元素化合价角度分析Na2O2的性质

2、强氧化性的五个表现