- 为您推荐:
 氢
氢
 仪器网
氢
仪器网
氢
氢(qīng)是一种化学元素,英文[hydrogen],化学元素符号为H,原子序数为1,在元素周期表中位于第一位。氢具有无色、无味、无臭等特点。氢通常的单质形态是氢气,它也是最轻的气体。
氢是由英国化学家卡文迪许在1766年发现,1787年法国化学家拉瓦锡证明氢是一种单质并命名。氢其原子质量为1.00794,是最轻的元素,也是宇宙中含量最多的元素,大约占据宇宙质量的75%。主星序上恒星的主要成分都是等离子态的氢,而在地球上,自然条件形成的游离态的氢单质相对罕见。
氢在自然界中分布很广,水便是氢的“仓库”。水中含11%的氢,泥土中约有1.5%的氢,石油、天然气、动植物体也含氢。在空气中,氢气倒不多,约占总体积的一千万分之五。
氢的物理性质
熔点:14.025 K (-259.125 ℃)
沸点:20.268 K (-252.882 ℃)
三相点:13.8033 K (-259 ℃)7.042kPa
临界点:32.97 K (-240 ℃) 1.293MPa
摩尔体积:22.4L/mol
汽化热:0.44936 kJ/mol
熔化热:0.05868 kJ/mol
蒸气压:209 帕斯卡(23K)
比热容量:14000J/(kg·℃)
声在其中传播的速度:1270 m/s(293.15K)
电离能(kJ /mol):M - M+ 1312
密度、硬度:0.0899 kg/m³(273K)、NA
热导率:W/(m·K)180.5
氢的化学性质
在常温下,氢比较不活泼,但可用合适的催化剂使之活化。在高温下,氢是高度活泼的。除稀有气体元素外,几乎所有的元素都能与氢生成化合物。非金属元素的氢化物通常称为某化氢,如卤化氢、硫化氢等;金属元素的氢化物称为金属氢化物,如氢化锂、氢化钙等。
氢的储存方法
氢是一种能量密度很高的清洁可再生能源,但其特殊性质导致难以常温常压储存,泄漏后有爆炸危险。保存氢气方法有很多,但是高效的储氢方法主要有:液化储氢(成本太高,而且需要很高的能量维持其液化);压缩储氢(重量密度和体积密度都很低);金属氢化物储氢(体积存储密度较高,但是重量密度低),还有一个是现在正在研究的碳纳米管吸附储氢。
氢的储运技术是制约氢能发展的最主要技术瓶颈,目前其研究主要集中在高压储氧罐、轻金属材料、复杂氢化物材料、有机液态材料等氢储运技术。将氢气经特殊处理溶解在液态材料中,实现氢能的常态化、安全化应用,甚至用普通矿泉水瓶也能装运,这一愿景正在逐渐接近现实。业界认为该技术处于国际领先水平,并有可能引发氢能利用革命。
氢的用途
氢是一种工业原料,如生产合成氨和甲醇,也用来提炼石油,氢化有机物质作为收缩气体,用在氧氢焰熔接器和火箭燃料中。在高温下用氢将金属氧化物还原以制取金属。氢还广泛用于钨、钼、钴、铁等金属粉末和锗、硅的生产。由于氢气很轻,人们利用它来制作氢气球——氢气球。氢气与氧气化合时,放出大量的热,被利用来进行切割金属。
氢的同位素
在自然界中,氢的同位素有:氕 (氢1)、氘 (氢2, 重氢)、氚 (氢3, 超重氢)。以人工方法合成的同位有:氢4、氢5、氢6、氢7。
氕的原子序数为1,原子量为1.007947,元素符号为H。
氘元素符号一般为D或2H,质量数2。它的原子核由一颗质子和一颗中子组成。
氚元素符号T或者3H,也被称为"超重氢"。原子核中有一个质子和两个中子。
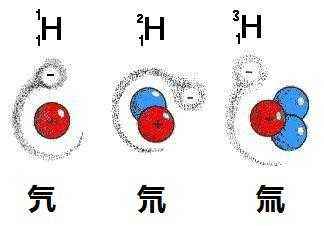
氢的同位素主要有三种,分别为氕(读piē)、氘(读dāo)、氚(读chuān),分别简写为H、D、T。氕(piē)氕为原子质量为1的普通的轻氢同位素,它是氢的主... [查看全部]
氢的同位素主要有三种,分别为氕(读piē)、氘(读dāo)、氚(读chuān),分别简写为H、D、T。
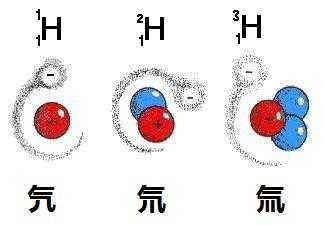
氕(piē)
氕为原子质量为1的普通的轻氢同位素,它是氢的主要成分。
氕通常称为氢,氕的原子序数为1,原子量为1.007947。天然丰度为99.985%,按原子百分数计,它是宇宙中最多的元素,在地球上的含量仅次于氧,它主要分布于水及各种碳氢化合物中。在常温下,它是无色无臭的气体。
氕是氢的主要稳定同位素,天然氢中氕占99.985%,因此,氕气适用于所有应用超纯氢的领域。氕不但是一种优质燃料,还是石油、化工、化肥和冶金工业中的重要原料和物料。石油和其他化石燃料的精炼需要氢,如烃的增氢、煤的气化、重油的精炼等;化工中制氨、制甲醇也需要氢。氢还用来还原铁矿石。用氢制成燃料电池可直接发电,采用燃料电池和氢气-蒸汽联合循环发电,其能量转换效率将远高于现有的火电厂。
氘(dāo)
氘为氢的一种稳定同位素,也被称为重氢。元素符号一般为D或2H,质量数2。它的原子核由一颗质子和一颗中子组成。在大自然的含量约为一般氢的7000分之一,用于热核反应。聚变时放出β射线后形成质量数为3的氦。氘被称为“未来的天然燃料”。
氘在常温常压下为无色无嗅无毒可燃性气体,是普通氢的一种稳定同位素。它在通常水的氢中含0.0139%~0.0157%。其化学性质与普通氢完全相同。但因质量大,反应速度小一些。氘于核能、可控核聚变反应、氘化光导纤维、氘润滑油、激光器、灯泡、实验研究、半导体材料韧化处理以及核医学,核农业等方面;另外在军事上,它也有一些重要的用途,比如制造氢弹,中子弹和DF激光武器。
氚(chuān)
氚为氢的放射性同位素,原子量为普通氢的三倍,半衰期12.5年,蜕变时放出β射线后形成质量数为三的氦。用中子轰击锂可产生氚。
氚元素符号T或者3H,也被称为"超重氢"。原子核中有一个质子和两个中子。并带有放射性,会发生β衰变,
... 查看全文氧化氢是什么,氧化氢即水,是民间人们对水的别称,又叫一氧化二氢。
氧化氢,化学式为H₂O,是由氢、氧两种元素组成的无机物,在常温常压下为无色无味的透明液体,被称为人类生命的源泉。
水有三种形态,分别为:固态、液态、气态。其次为超临界流体、超固体、超流体、费米子凝聚态、等离子态、玻色-爱因斯坦凝聚态等等。水(液体)0℃时会冻成冰(固体)。加热到100°C时水会沸腾,变成肉眼看不见的水蒸气(气体)。
水的物理性质
通常水是无色、无味的液体。
沸点:99.975℃(气压为一个标准大气压时,也就是101.375kPa)。
凝固点:0℃
三相点:0.01℃
最大相对密度时的温度:3.982℃
比热容:4.186kJ/(kg·℃) 0.1MPa 15℃蒸发潜热:2257.2kJ/(kg) 0.1MPa 100℃
密度:水的密度在3.98℃时最大,为1×103kg/m3,水在0℃时,密度为0.99987×103 kg/m3,冰在0℃时,密度为0.9167×103 kg/m3。
临界温度:374.2℃
导热率:在20℃时,水的热导率为0.006 J/s·cm·K
冰的热导率为0.023 J/s·cm·K
在雪的密度为0.1×103 kg/m3时,雪的热导率为0.00029 J/s·cm·K
水的化学性质
稳定性:水在在2000℃以上才开始分解
纯水中存在下列电离平衡:H₂O==可逆==H⁺+OH⁻ 或 H₂O+H₂O=可逆=H₃O⁺+OH⁻。
氧化性:水跟较活泼金属或碳反应时,表现氧化性,氢被还原成氢气。
2Na+2H₂O=2NaOH+H₂↑
Mg+2H₂O=Mg(OH)₂↓+H₂↑
3Fe+4H₂O(水蒸气)=Fe₃O₄+4H₂(加热)
C+H₂O=CO+H₂(高温)
还原性:水跟氟单质反应时,表现还原性,氧被还原成氧气。
2F₂+2H₂O=4HF+O₂↑
水的电解:水在直流电作用下,分解生成氢气和氧气,工业上用此法制纯氢和纯氧。
2H₂
... 查看全文