-
公司新闻
-
Wes助力北京理工大学连发两篇外泌体权威论著
发布:ProteinSimple, a biotechne brand浏览次数:609北京理工大学生命科学学院的科学家,利用全自动定量Western Blot系统 Wes,在化学领域的国际yi流期刊Angewandte Chemie International Edition(IF:12.257)连续发表两篇外泌体相关论文,研究M2巨噬细胞来源外泌的KY作用及其机制。
论文一
Molecularly Engineered Macrophage-Derived Exosomes With Inflammation Tropism and Intrinsic Heme Biosynthesis for Atherosclerosis Treatment, Angew Chem Int Ed Engl. 2020 Mar2;59(10):4068-4074.
--研究背景--
心血管疾病是发病率和死亡率的主要原因之一,而动脉粥样硬化是心血管疾病的主要诱因。而炎症不仅是动脉粥样硬化的主要指征,而且还驱动着整个疾病的发展。因此,KYZL被认为是ZL动脉粥样硬化的一种有前途的ZL策略。但现有的临床抗动脉粥样硬化药物缺乏针对炎症部位的特异性靶向能力,以及较差的半衰期,这不仅降低了药物的实际ZL功效,而且还会导致了许多副作用,甚至死亡。
纳米颗粒作为一种新型的药物递送系统,可以伴随着脉管系统渗漏,被动地积聚在病理区域。但纳米颗粒载体本身的免疫原性和毒性,以及快速的免疫识别,血液清除和不良的体内生物分布,导致靶向ZL动脉粥样硬化KY药物的研发仍具有挑战性。
外泌体,直径为30-150nm的纳米囊泡,具有出色的生物相容性,低细胞毒性,低免疫原性,特异性靶向和长时循环能力,使其成为有效的药物输送工具。除此之外,因内涵源自亲代细胞的特定内容物(例如RNA,DNA,蛋白质和小分子),外泌体可以将来源于原始细胞的天然生物学功能直接用于疾病ZL。例如,源自心脏祖细胞的外泌体,可以增强心肌梗塞后的心脏功能。有文章报道,M2表型巨噬细胞可以分泌KY细胞因子,例如白介素10(IL-10),白介素1Ra(IL-1Ra)和转化生长因子(TGF-β),暗示由M2巨噬细胞分泌的外泌体(M2 Exo)可能具有潜在的KYZL作用。
HAL(5-氨基乙酰丙酸己酯盐酸盐):通过酶法合成中间体原卟啉IX(PpIX),之后转化为血红素,血红素有效地转化为分解代谢产物CO和胆红素,从而产生KY作用。
因此本文旨在探讨,负载KY药物HAL的M2巨噬细胞分泌的外泌体,是否对动脉粥样硬化产生KY效果。
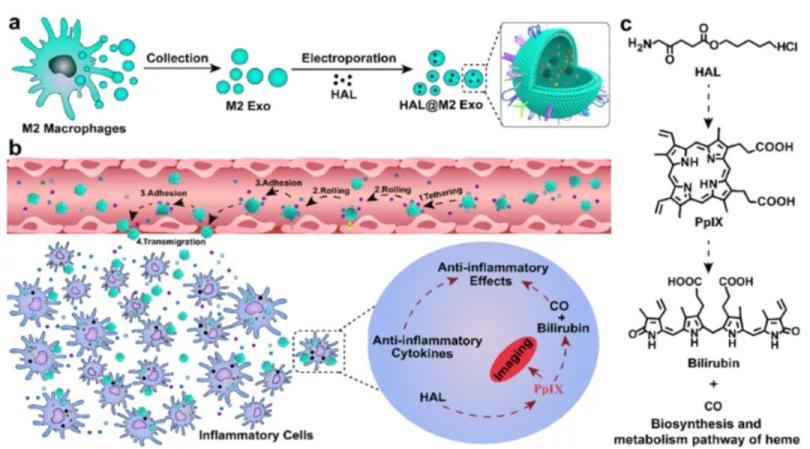
负载HAL的M2外泌体(HAL@M2 Exo)的制备及表征
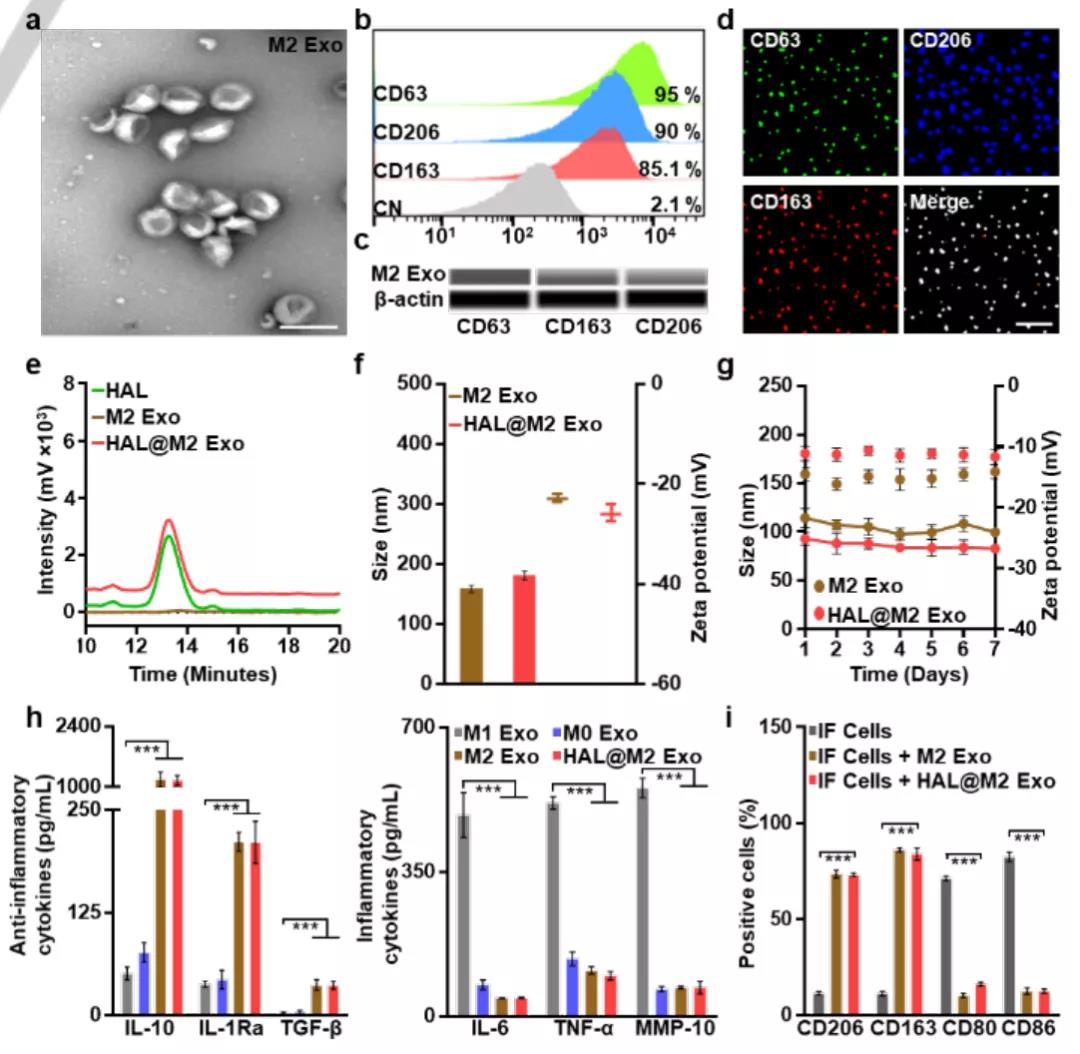
利用Wes,与电镜技术、流式细胞术以及免疫荧光实验,共同验证了M2巨噬细胞的biomarker:CD163, CD206和外泌体biomarker:CD63。随后实验验证了M2外泌体良好的负载能力,以及负载HAL后的未发生改变的表面特性,以及的胶体稳定性。同时检测M2 Exo 和HAL@M2 Exo分泌KY细胞因子的能力,以及YZ促炎细胞因子的产生,同时可以诱导促炎M1巨噬细胞的重编程。
HAL可以在细胞中诱导血红素的GX生物合成和代谢
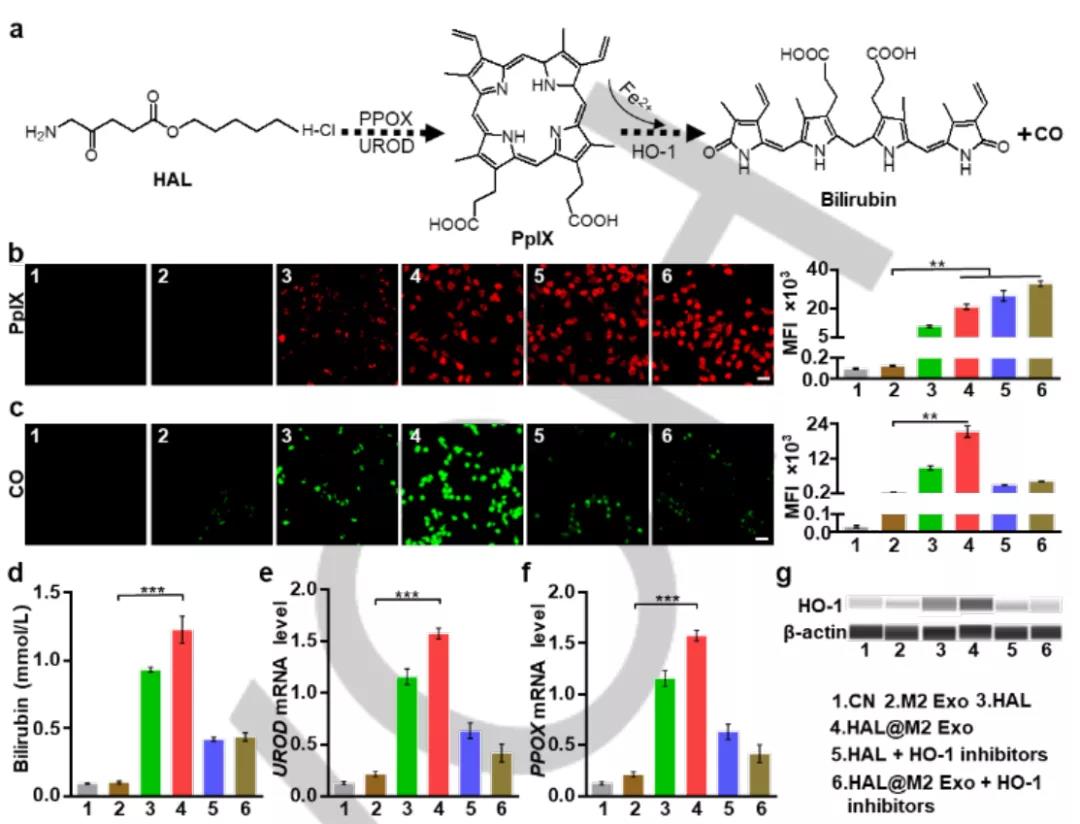
利用Wes检测,结果显示HAL和HAL@M2 Exo的HO-1水平显著升高,与此同时,中间体PpIX和产物CO和胆红素的升高,以及与其相关的生物合成酶尿卟啉原脱羧酶(UROD)和原卟啉原氧化酶(PPOX)的升高,共同验证了外源HAL分子可以显着增强酶催化的血红素的生物合成和代谢,同时生成相应的功能性中间体和代谢产物。
HAL@M2 Exo出色的炎症亲和力
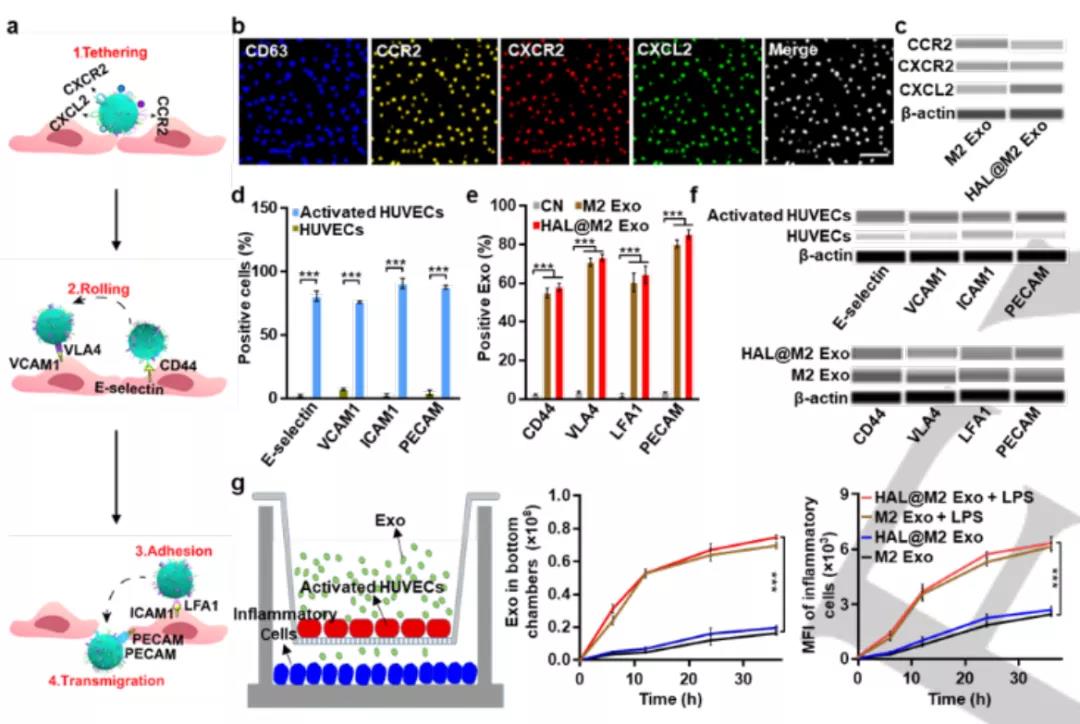
利用Wes检测,结果验证了M2 Exo和HAL@M2 Exo中,三种趋化因子受体的存在,包括CC趋化因子受体2(CCR2),CXC趋化因子受体2(CXCR2)和CXC趋化因子配体2(CXCL2),说明它将对炎症刺激产生了响应,从而导致基于M2 Exo的纳米载体的减慢和募集。同时,活化的人脐静脉内皮细胞(HUVECs)上的E-选择蛋白,血管细胞粘附分子1(VCAM1)和内皮细胞间粘附分子1(ICAM1)表达增加,M2 Exo和HAL@M2 Exo显示出趋化因子受体包括CD44,单核细胞晚期抗原4(VLA4)和M2 Exo膜上存在的单核细胞淋巴细胞功能相关抗原1(LFA1)高水平的表达,表明HAL@M2 Exo与活化的HUVECs之间具有很强的分子识别能力。血小板内皮细胞粘附分子(PECAM)是内皮细胞跨膜蛋白之一,在调节迁移过程中起着重要的作用,它在M2 Exo的纳米载体和活化的HUVECs上高表达,说明基于M2 Exo的纳米载体在炎症部位的出色迁移和积累。
HAL@M2 Exo的体外增强KY作用
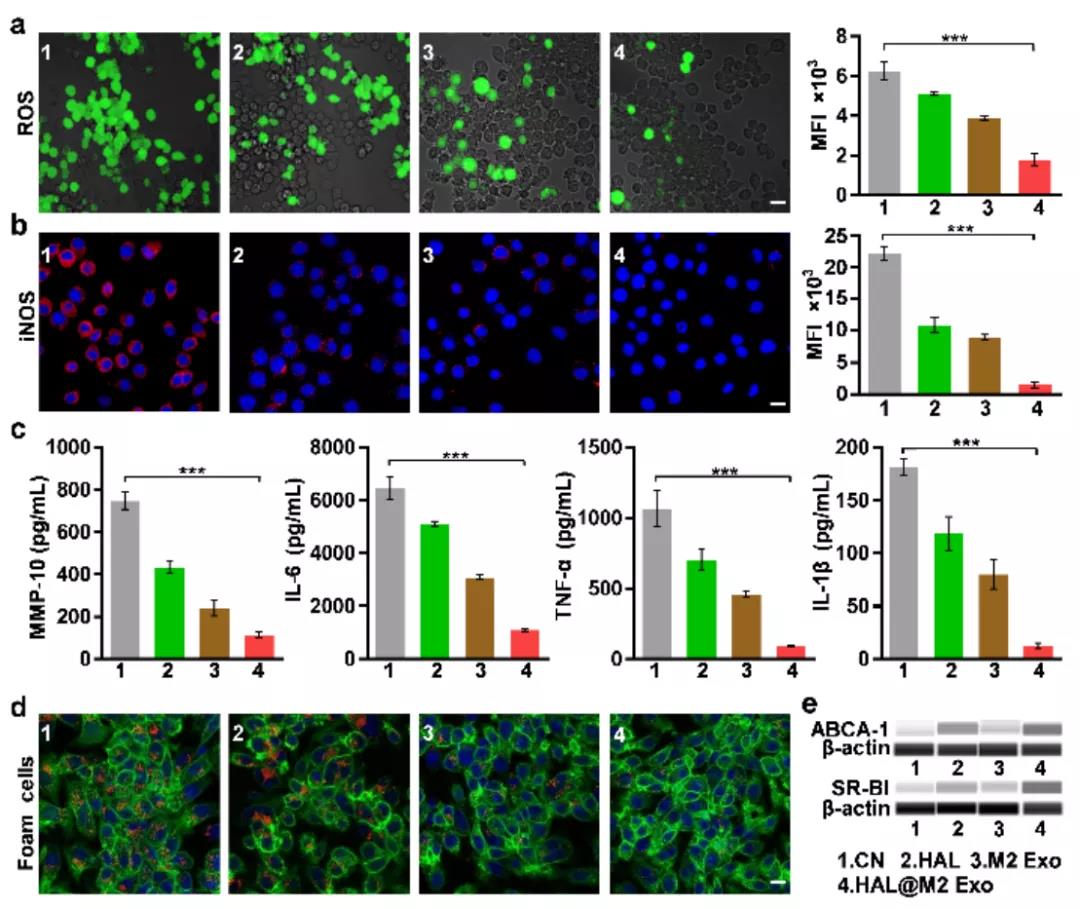
利用Wes检测,结果显示,负责胆固醇的反向转运(RCT)途径的两个受体(SR-BI和ABCA-1)在HAL和HAL@M2 Exo中的表达上调,表明二者均可以促进泡沫细胞中的胆固醇外流。同时也验证了HAL@M2 Exo出色的抗活性氧族以及KY症因子的作用。
HAL@M2 Exo在急性腹膜炎中的体内KYZL
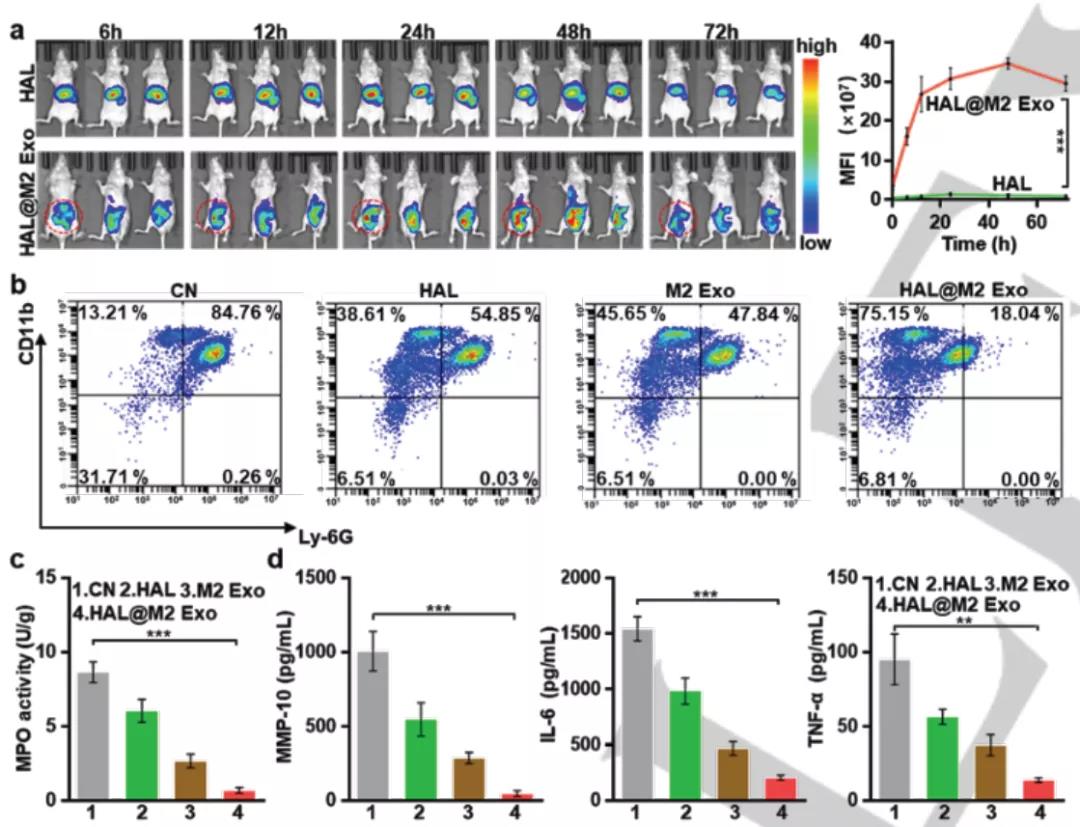
在小鼠急性腹膜炎模型中,HAL@M2 Exo可以jing准定位到炎性组织,且有效地减少浸润性中性粒细胞在腹腔中的保留,下调了炎症因子MMP-10,IL-6,TNF-α,IL-1β的水平,降低MPO活性。
HAL@M2 Exo在体内可有效ZL早期动脉粥样硬化
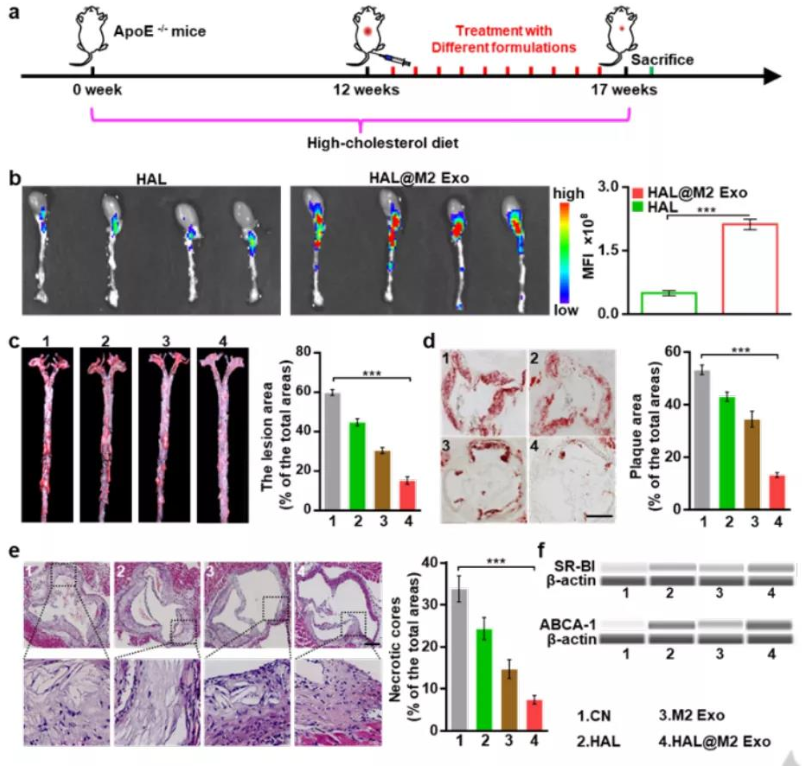
利用Wes,检测到在早期动脉粥样硬化的小鼠模型中,负责胆固醇的反向转运(RCT)途径的两个受体(SR-BI和ABCA-1)在HAL和HAL@M2 Exo中表达上调,与体外实验吻合。同时也验证了HAL@M2 Exo的炎症定位倾向和有效减少了炎症引起的主动脉病变面积。
论文二
Responsive Exosome Nano-bioconjugates for Synergistic Cancer Therapy, Angew Chem Int Ed Engl. 2020 Jan 27;59(5):2018-2022.
--研究摘要--
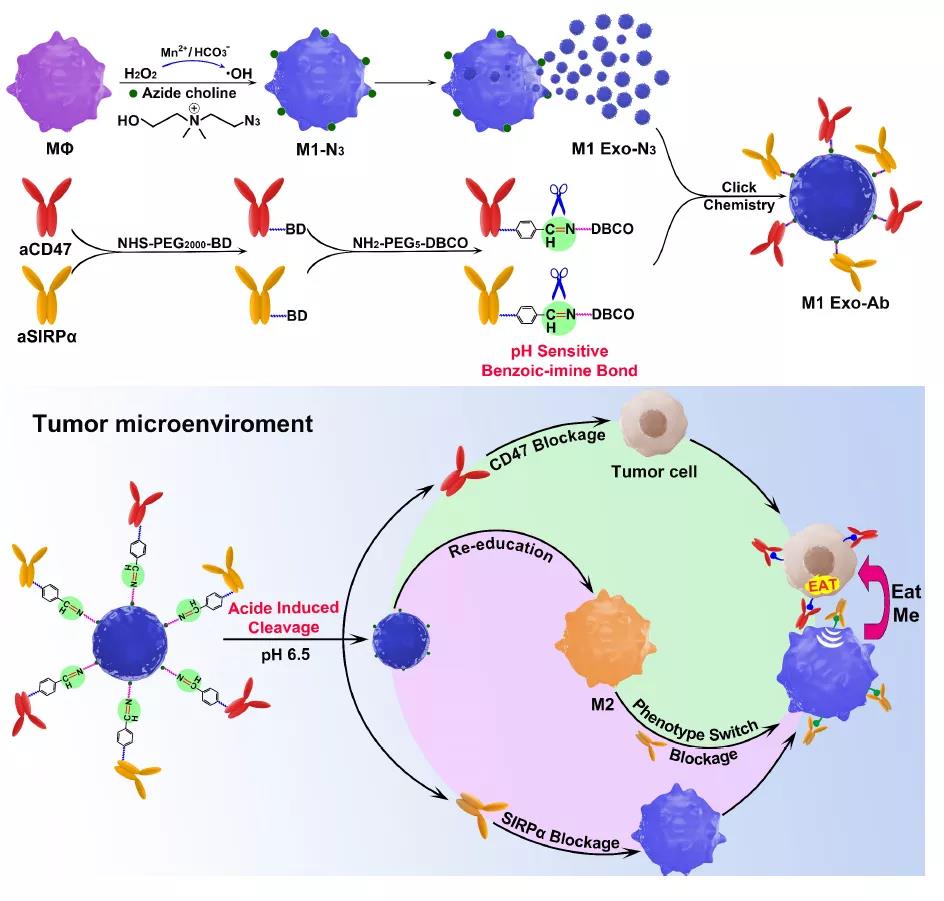
外泌体在药物ZL中具有巨大潜力。然而,天然外泌体通常在体内发挥的作用有限,并且仅充当药物递送载体。本研究中合成了用于癌症ZL的反应性外泌体纳米生物共轭物。通过pH敏感的连接子,将M1巨噬细胞衍生的叠氮化物修饰的外泌体与CD47和SIRPα(aCD47和aSIRPα)的二苯并环辛炔修饰的抗体缀合。全身给药后,纳米生物共轭物可以通过肿瘤细胞表面上aCD47和CD47之间的特异性识别来主动靶向肿瘤。在酸性肿瘤微环境中,纳米生物共轭物的苯甲酸-亚胺键断裂,释放出aSIRPα和aCD47,它们可以分别阻断巨噬细胞和CD47上的SIRPα,从而消除“不吃我”的信号,并改善巨噬细胞的吞噬作用。同时,天然M1外泌体可以有效地将巨噬细胞从促肿瘤M2重编程为抗肿瘤M1。因此,外泌体生物缀合物可以发挥协同的作用。

本文利用Wes检测,结果显示Mn2+处理后巨噬细胞中磷酸p-NF-κB p65(p-p65)的表达迅速增加,后续结果验证了Mn2+通过•OH介导的NF-κB活化,诱导了M1的极化。
Wes/Jess全自动定量Western Blot系统

国内其他实验室使用Wes/Jess系统发表外泌相关论著:
1.Pengcheng Wang et al,Plasma Exosome-derived MicroRNAs as Novel Biomarkers of Traumatic Brain Injury in Rats,Int. J. Med. Sci. 2020, Vol. 17
2.Ying Wang et al, Expression and functional regulation of gap junction protein connexin 43 in dermal mesenchymal stem cells from psoriasis patients,Acta Histochemica, 2020
3.Linsen Ye et al,Tumor-derived exosomal HMGB1 fosters hepatocellular carcinoma immune evasion by promoting TIM-1+ regulatory B cell expansion,Journal for ImmunoTherapy of Cancer (2018) 6:145
4.GUANQUN ZHU et al,Acute effect of lactic acid on tumor-endothelial cell metabolic coupling in the tumor microenvironment,ONCOLOGY LETTERS 12: 3478-3484, 2016
(来源:ProteinSimple)
2020-06-29 -
免责声明
①本网刊载上述内容,并不代表本网赞同其观点或证实其内容的真实性,不承担此类作品侵权行为的直接责任及连带责任
②若本站内容侵犯到您的合法权益,请及时告诉,我们马上修改或删除。邮箱:hezou_yiqi

-
 认证会员 第
6 年
认证会员 第
6 年ProteinSimple, a biotechne brand
认证:工商信息已核实
- 产品分类
- 品牌分类
-
仪企号
 ProteinSimple, a biotechne brand
ProteinSimple, a biotechne brand
-
友情链接
-
手机版开启全新的世界m.yiqi.com/zt3162/




