-
产品文章
-
电解池及其应用
发布:天津市兰力科化学电子高技术有限公司浏览次数:2288一、电解池的构成条件
1.定义:
电解池是将电能转化成化学能的装置。电流通过电解质溶液(或熔融的电解质)而在阴、阳两极引起氧化还原反应的过程。
2.构成条件
电源——通常为直流电源
电极——两个电极插入电解质溶液或熔融态电解质
电路——形成闭合回路
二、电解池的工作原理
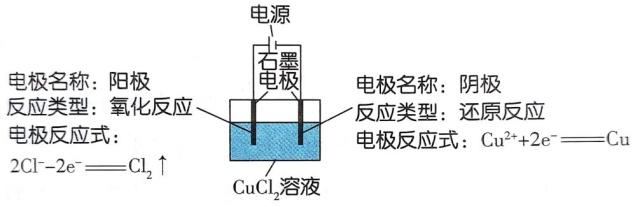
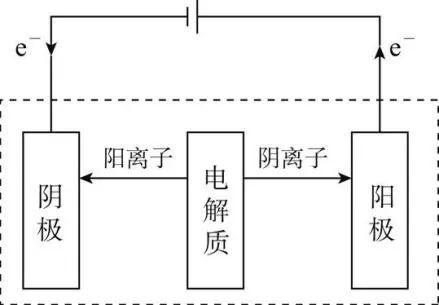
负阴得还
电源负极
连接阴极
发生得电子的
还原反应
正阳失氧
电源正极
连接阳极
发生失电子的
氧化反应
三、电解时离子的放电顺序(电解池电极反应式书写)
注意事项
☆惰性电极:Pt、Au、石墨
☆活泼电极:除了惰性电极以外的其他常见金属材料,放电时生成对应金属离子,如Fe - 2e-=Fe2+
☆氧化性越强的越优先发生还原反应,还原性越强的越优先发生氧化反应
☆OH-不区分碱电离和水电离,碱电离4OH- - 4e-=2H2O + O2↑,水电离2H2O - 4e-=O2↑+ 4H+
☆金属离子放电一般生成对应的金属,如:Cu2+ + 2e-=Cu
☆H+放电生成氢气2H+ + 2e-=H2 ,Cl-、Br-、I-、S2-放电生成Cl2、Br2、I2、S
☆书写电解池中电极反应式时,如果氢离子来自于水,那电极反应式写水或氢离子都可以,但书写电解总反应方程式时,要写水分子。(OH-相同)
☆阴极材料主要作用是导电,电极本身一般不反应,是溶液(或熔融电解质)中的阳离子放电。
☆要确保两极电子转移数目相同,且总反应方程式中注明条件“电解”。
☆电解水溶液时,应注意放电顺序中H+、OH-之后的离子一般不参与放电。
实例:
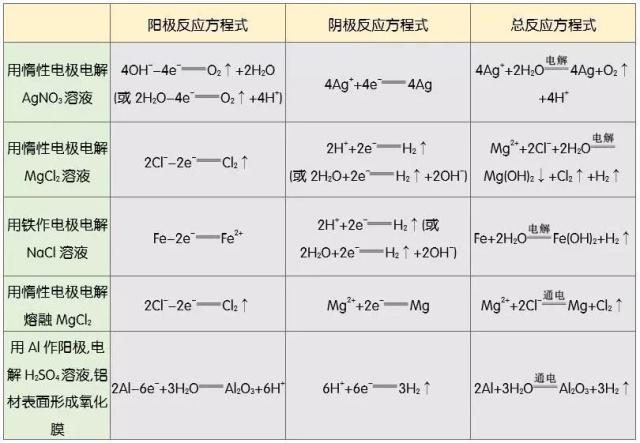

四、以惰性电极电解电解质溶液的规律
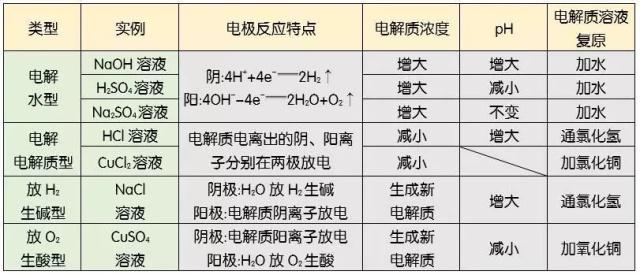
五、电解原理在工业生产中的应用
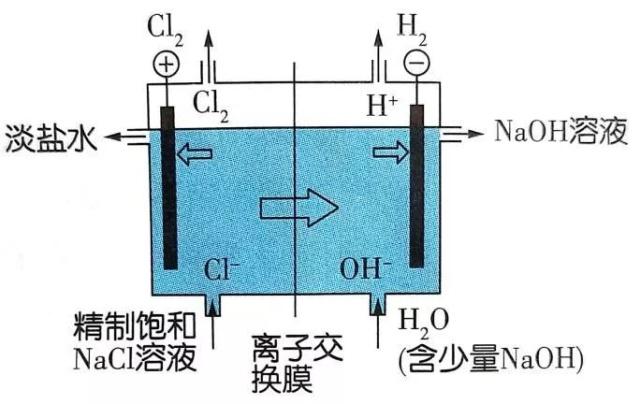
1.氯碱工业(电解饱和食盐水制烧碱、氯气和氢气)
阳极: 2Cl--2e-Cl2↑
阴极: 2H++2e-H2↑(或2H2O+2e-H2↑+2OH-)
总反应:2NaCl+2H2O2NaOH+H2↑+ Cl2↑
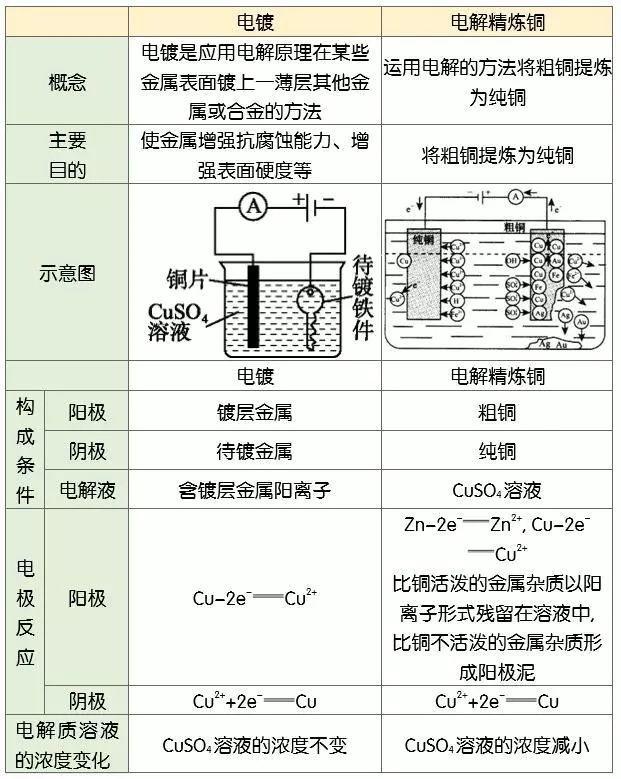
2.电镀与电解精炼
3.电冶金

电解原理应用中的注意点
①阳离子交换膜(以电解NaCl溶液为例),只允许阳离子(Na+)通过,而阻止阴离子(Cl-、OH-)和分子(Cl2)通过,这样既能防止H2和Cl2混合爆炸,又能避免Cl2和NaOH溶液作用生成NaClO影响烧碱质量。
②电解或电镀时,电极质量减少的电极必为金属电极——阳极;电极质量增加的电极必为阴极,即溶液中的金属阳离子得电子变成金属吸附在阴极上。
③电解精炼铜,粗铜中含有的Zn、Fe、Ni等活泼金属失去电子,变成金属阳离子进入溶液,其活泼性小于铜的杂质以阳极泥的形式沉积。电解过程中电解质溶液中的Cu2+浓度会逐渐减小。
④电镀时,阳极(镀层金属)失去电子的数目跟阴极镀层金属离子得到电子的数目相等,电镀液的浓度保持不变。
六、电化学的有关计算
 2020-06-16相关仪器
2020-06-16相关仪器 -
免责声明
①本网刊载上述内容,并不代表本网赞同其观点或证实其内容的真实性,不承担此类作品侵权行为的直接责任及连带责任
②若本站内容侵犯到您的合法权益,请及时告诉,我们马上修改或删除。邮箱:hezou_yiqi

-
 认证会员 第
5 年
认证会员 第
5 年天津市兰力科化学电子高技术有限公司
认证:工商信息已核实
- 产品分类
- 品牌分类
-
仪企号
 天津市兰力科化学电子高技术有限公司
天津市兰力科化学电子高技术有限公司
-
友情链接
-
手机版开启全新的世界m.yiqi.com/zt72585/






