Orbitrap高分辨质谱在生物药物研发和质量控制中的应用
从早期研发、表征分析、工艺优化到CMC、QC 分析,生物药在每一个环节均存在着复杂性和不确定性,赛默飞高分辨质谱生物制药解决方案提供稳定准确的分析方法,为您的药品申报上市保驾护航。
一、蛋白表征分析
01一级结构分析
分子量测定
基于Orbitrap超高分辨质谱测得的分子量更接近实际值,且能够准确分辨质量相近的成分[1,2],以更加严格的标准表征蛋白。
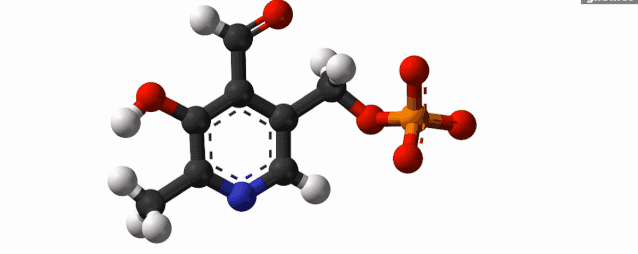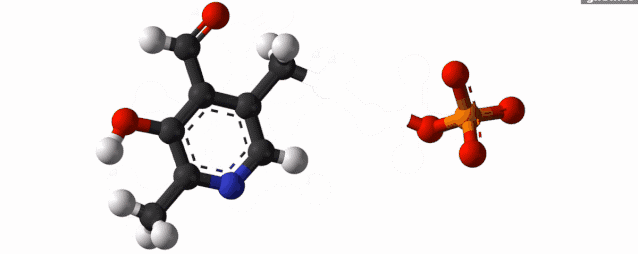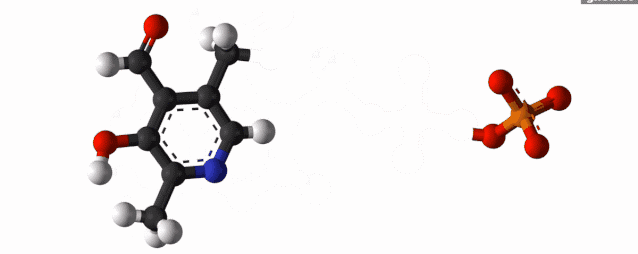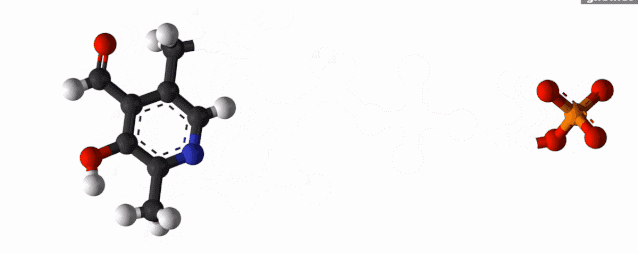
02一级结构分析
肽图分析
一级结构分析—肽图分析,生物药的氨基酸序列是其生物活性、临床LX的物质基础,确保序列与预期一致是S要条件。且氨基酸的翻译后修饰可能会影响其亲和力和生物学活性,鉴定修饰的类型和位置可作为生物药CQA评定的重要指标。
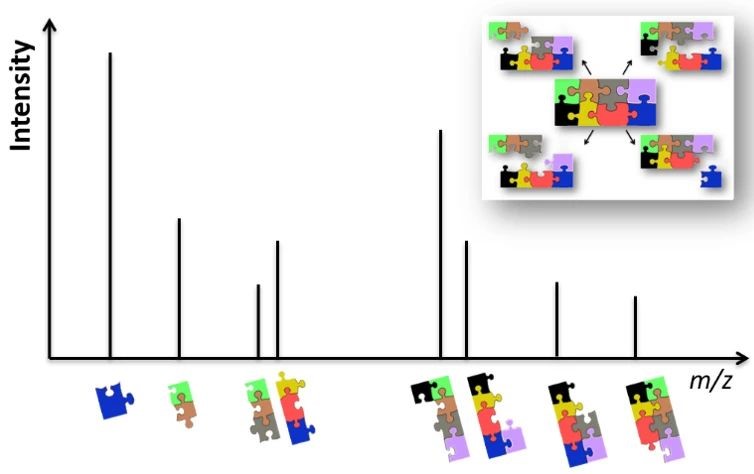
图1. Orbitrap能够获得多肽更加准确的一级极ng确质量和二级丰富的碎片离子
通过Orbitrap超高分辨质谱仪能够获得多肽更加准确的一级极ng确质量和丰富的二级碎片信息,为生物药的氨基酸和翻译后修饰表征提供强有力的支撑。
03一级结构分析
糖型分析
一级结构分析—糖型分析,糖基化对生物药的LX、稳定性、免疫原性具有重要的影响。面对结构极为复杂的寡糖,赛默飞集结优势产品解决这一难题。
方案一、游离糖型LC-MS分析完整解决方案
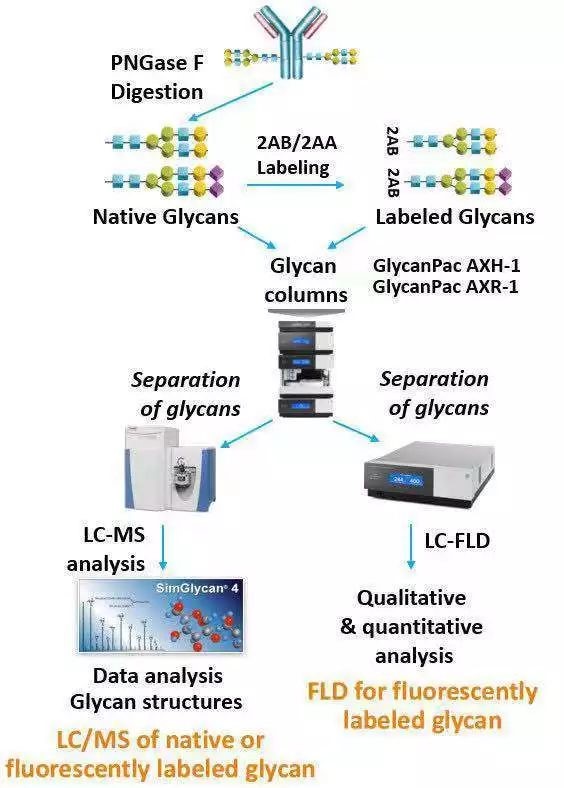
经典的LC-MS分析流程,释放糖链,糖链标记,荧光对糖链进行定量,高分辨质谱进行糖链结构鉴定。
方案二、游离糖型IC-MS分析完整解决方案

对于高含量的唾液酸蛋白,2AB标记过程中会导致脱唾液酸化[3],而赛默飞优势产品离子色谱和质谱联用的方案无需糖型衍生化复杂的样品前处理过程,实现对未衍生化糖型的直接定量和定性,减少样品在标记过程中唾液酸的降解。
04高级结构分析
氢氘交换质谱法(HDX-MS)
高级结构分析—氢氘交换质谱法(HDX-MS),对样品的要求比较低,不需要结晶,溶液状态即可;对缓冲盐,辅料等干扰物质的容忍性比较高;可以保证蛋白或者蛋白复合物在天然非变性状态下进行测定;能够实现从完整水平、局部水平以及单个氨基酸的水平上获得详细信息,使得Z终的蛋白质高级结构的信息更加全面和准确。
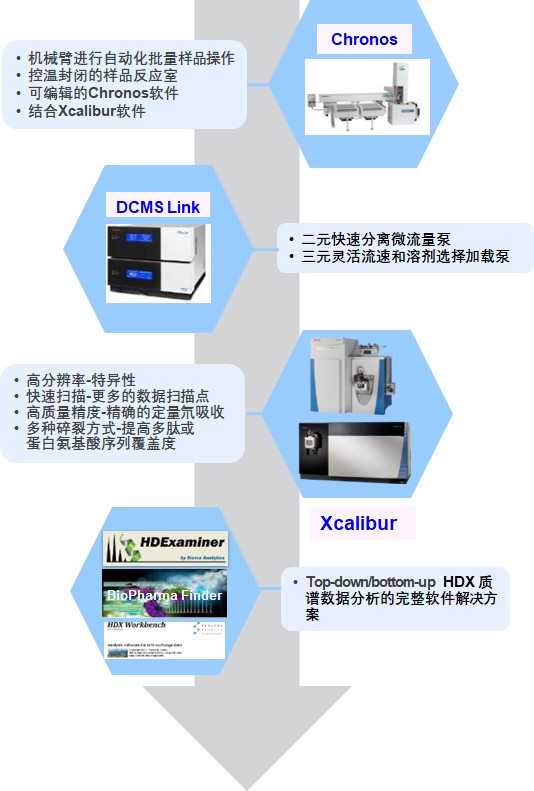
图2.氢氘交换质谱法完整解决方案
二、生物药宿主细胞残留蛋白(HCPs)分析
HCPs的存在主要影响药物的安全性和有效性,基于Orbitrap高灵敏度和宽的动态范围,可实现对未知HCPs的高通量定性和定量。与ELISA方法相比开发周期更短,兼顾定性和定量,图3为针对极低含量HCPs的完整解决方案。
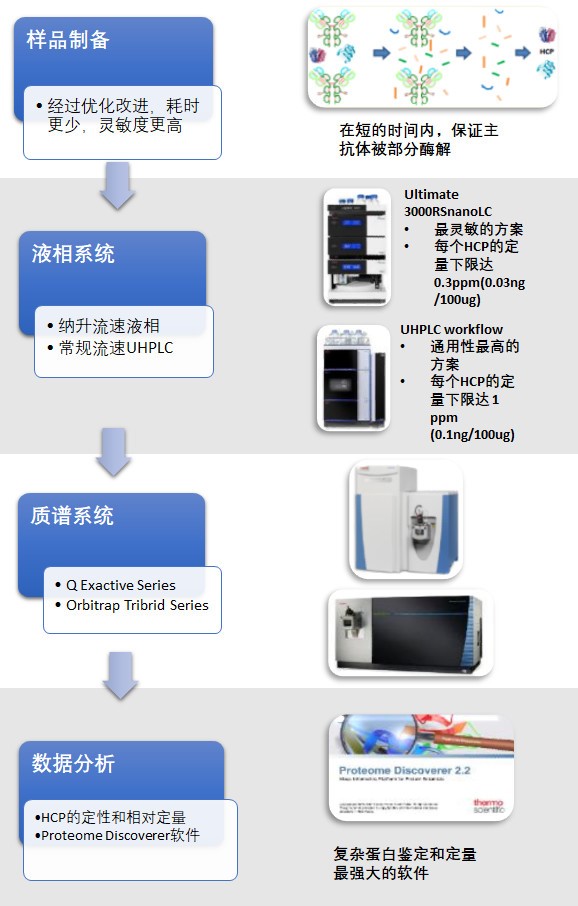
图3.基于LC-MS/MS方法对低含量的HCPs进行准确的定性和定量
三、生物药的生物分析
对于大分子的生物药而言,基于质谱定量方法相比于Ligand Binding Assays方法具有同时定性和定量、高特异性、开发周期短的优势;与三重四极杆质谱相比,除具有可媲美的定量能力外,能够监测生物药体内生物转化的优势。针对生物药完整蛋白水平和多肽水平定量的完整解决方案如图4,其定量限和线性范围远高于实际需求。

图4.基于LC-MS和LC-MS/MS对重组生物药生物分析的完整解决方案
四、多质量属性方法工作流程MAM
1个工作流程:
HR MAM是1个高分辨率高质量精度,实现从研发直至质量控制(QC)阶段产品质量属性的全面表征和监控的工作流程。
2个软件:
其中包含2个软件:Biopharma Finder找出关键质量属性,Chromeleon变色龙实现仪器控制及数据采集分析并具备强大的合规性。
3个要素:
3个要素:质量属性表征;质量属性监控以及未知组分检测。Z终实现一套方案能够实现多种传统分析方法检测结果,真正的化繁为简。
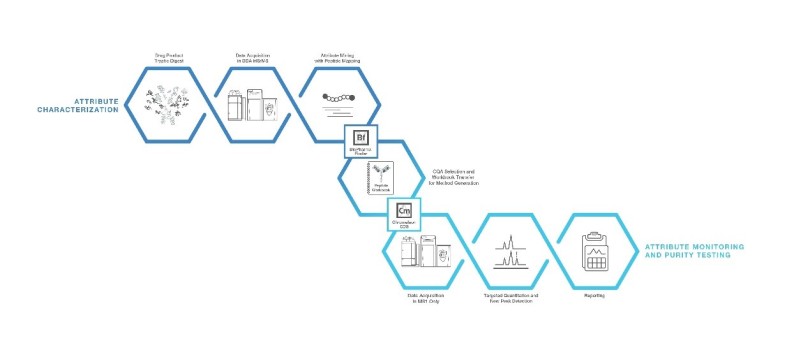
图5. 基于Orbitrap超高分辨质谱的多重关键质量属性(HR-MAM)完整解决方案
目前某国际创新生物制药巨头已将HR MAM用于质量控制阶段[4],以及美国监管机构Z近在AC上发表对MAM方法的评估[5],极大推进高分辨质谱用于生物药在生产质量控制实际应用的进程。
总结
基于Orbitrap超高分辨质谱仪于生物制药的完整解决方案,GX、快速、准确, 从药物表征到生产流程全方wei助力新药上市。
参考资料:
[1]. He J, Su D, Ng C, et al. High-resolution accurate-mass mass spectrometry enab领 in-depth characterization of in vivo biotransformations for intact antibody-drug conjugates[J]. Analytical chemistry, 2017, 89(10): 5476-5483.
[2]. Schachner L, Han G, Dillon M, et al. Characterization of chain pairing variants of bispecific IgG expressed in a single host cell by high-resolution native and denaturing mass spectrometry[J]. Analytical chemistry, 2016, 88(24): 12122-12127.
[3]. Szabo Z, Thayer J R, Reusch D, et al. High performance anion exchange and hydrophilic interaction liquid chromatography approaches for comprehensive mass spectrometry-based characterization of the N-glycome of a recombinant human erythropoietin[J]. Journal of proteome research, 2018, 17(4): 1559-1574
[4]. Rogers R S, Night领er N S, Livingston B, et al. Development of a quantitative mass spectrometry multi-attribute method for characterization, quality control testing and disposition of biologics[C]//MAbs. Taylor & Francis, 2015, 7(5): 881-890.
[5]. Rogstad S, Yan H, Wang X, et al. Multi-Attribute Method for Quality Control of Therapeutic Proteins[J]. Analytical Chemistry, 2019, 91(22): 14170-14177.
扫描下方二维码即可获取赛默飞全行业解决方案,或关注“赛默飞色谱与质谱中国”公众hao,了解更多资讯+

全部评论(0条)
推荐阅读
-
- 【线上课程】报名赢好礼!“高分辨质谱在ADC抗体药物中的全面表征方案”即将开播!
- 3月20日19:30,与您线上相约!
-

- 沃特世于ASMS推出全新高分辨质谱产品和软件,加速药物研发
- 全新Xevo G3 QTof系统是一款高性能台式质谱仪,可用于对生物治疗药物、法医学、代谢物鉴定、代谢组学以及可萃取物和可浸出物等应用中的分子进行表征和量化。
-
- 颠覆认知,“质“的飞跃|Orbitrap Astral高分辨质谱仪再次亮相厦门代谢组学大会
- 颠覆认知,“质“的飞跃|Orbitrap Astral高分辨质谱仪再次亮相厦门代谢组学大会
-

- 【讲座预告】质谱在工业诊断、问题溯源中的应用指南
- 讲座时间:2022年8月25日(星期四), 19:30 - 20:30
-

- CGT药物研发及生产流程的质量安全控制策略
- CGT药物研发及生产流程的质量安全控制策略
①本文由仪器网入驻的作者或注册的会员撰写并发布,观点仅代表作者本人,不代表仪器网立场。若内容侵犯到您的合法权益,请及时告诉,我们立即通知作者,并马上删除。
②凡本网注明"来源:仪器网"的所有作品,版权均属于仪器网,转载时须经本网同意,并请注明仪器网(www.yiqi.com)。
③本网转载并注明来源的作品,目的在于传递更多信息,并不代表本网赞同其观点或证实其内容的真实性,不承担此类作品侵权行为的直接责任及连带责任。其他媒体、网站或个人从本网转载时,必须保留本网注明的作品来源,并自负版权等法律责任。
④若本站内容侵犯到您的合法权益,请及时告诉,我们马上修改或删除。邮箱:hezou_yiqi


















参与评论
登录后参与评论