-
 过氧化氢 过氧化氢含量的测定
过氧化氢 过氧化氢含量的测定
 过氧化氢 过氧化氢含量的测定
过氧化氢 过氧化氢含量的测定
双氧水(过氧化氢,化学式H2O2),是一种重要的无机化工产品,也是工业领域重要的氧化剂、漂白剂、消毒剂和脱氯剂。在纺织、造纸、化工、轻工、医药、电子、食品、环保等领域应用广泛。目前我国双氧水产品分工业级、试剂级、医药级和电子级,浓度有27.5%,35%,50%,70%等多种规格。
过氧化氢含量的测定
H2O2在化学工业、医药工业、印染工业和食品行业等领域有着广泛的应用,可作为氧化剂、消毒剂、漂白剂等使用。但H2O2在使用的过程中会产生一些羟基自由基,具有很强的氧化性,对人体有一定危害。近年来,H2O2在环境中也普遍存在,因此对H2O2的检测具有重要的意义。检测H2O2的方法主要有:分光光度法、滴定法、电化学法、色谱法、化学发光法、共振散射光谱法、荧光光度法、原子吸收光谱法等。
荧光光度法测定过氧化氢
(一)实验部分
1、仪器和试剂
Cary Eclipse型荧光分光光度计。
H2O2储备溶液:取2mL30% H2O2稀释至500mL,用KMnO4法标定得准确浓度为4.06×10-2mol/L;
H2O2工作溶液:1.624×10-4mol/L(临用前用储备溶液稀释);
NaOH溶液:1mol/L;
邻苯二胺:2×10-3mol/L;
四羧基铁酞菁(FeC4Pc)0.0186g用3.5mL 0.2mol/L NaOH溶液溶解,用水定容至250mL,得到浓度为1.0×10-4mol/L。
所用试剂均为分析纯,实验用水均为二次去离子水。
2、实验方法
在2支5mL刻度试管中,分别加入0.2mL NaOH,0.1mL FeC4Pc,0.4mL OPDA,其中1支管中加入一定量的H2O2工作液,用水稀释至5mL,摇匀,静置80min。然后在荧光光度计上用1cm石英比色皿,设置电压为700V,狭缝宽度为10nm,激发波长为423nm,发射波长为577nm,分别测定加有H2O2的溶液的荧光值F和不加H2O2的试剂空白的荧光值F0,计算△F=F-F0。
(二)结果与讨论
1、体系的激发光谱和发射光谱
固定λem扫描体系的激发光谱,当发射波长为577nm时,体系在423nm处产生一个较强的激发峰;固定体系的激发波长λex时,体系在577nm处产生一个较强的荧光峰。体系的激发光谱和发射光谱见下图,体系的荧光波长选择577nm。
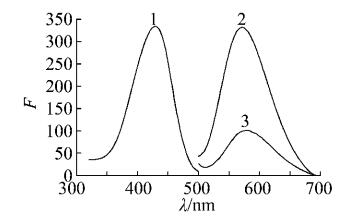
1:FeC4Pc+OPDA+H2O2激发光谱; 2:FeC4Pc +OPDA + H2O2发射光谱; 3: FeC4Pc+OPDA 发射光谱
2、实验条件的选择
①NaOH用量按实验方法进行实验,结果表明:1mol/L NaOH溶液加入量在0.1~0.5mL范围内荧光峰较好,荧光增加值△FZ大且基本不变,因此选择NaOH溶液的加入量为0.2mL。
②FeC4Pc用量 考察了FeC4Pc用量对体系的影响,实验结果表明:不加FeC4Pc时,△F值很小,几乎没有反应;随FeC4Pc加入量的增加,△F值逐渐增大,当FeC4Pc用量为0.1mL时,体系的△F值Z大,大于0.1mL后,△F值随其用量增加而逐渐减少,因此选择加入0.1mL 1.0×10-4mol/L FeC4Pc。
③OPDA用量 OPDA用量实验结果表明:随着OPDA体积的增大,体系△F值逐渐增大,当在0.3~0.6mL范围内,体系的△F值Z大且稳定,选择加入0.4mL 2×10-3mol/L OPDA。
④反应温度 在上述实验条件下,催化反应在室温即可进行,既可以减少酶活性的丧失,又可以避免H2O2在高温下分解。
⑤体系的稳定性 在室温下,体系的△F值在10~80min逐渐增大,在80min后趋于稳定,△F值在1h左右变化不大。因此实验选择在80min后进行测定。
3、标准曲线
在Z佳条件下,H2O2浓度在1.6×10-7~9.7×10-6mol/L范围内与△F值存在良好的线性关系。线性回归方程为:△F=2.199×107c+9.180(c为H2O2的浓度,单位为mol/L),相关系数为r=0.9941。按实验方法平行测定空白11次,标准偏差s为0.81,根据3s/k(k是标准曲线的斜率)计算出方法的检出限为1.1×10-7mol/L。
4、共存物质的干扰
当H2O2浓度为3.248×10-6mol/L(即0.11μg/mL)时,考察了可能存在干扰的物质对测定结果的影响。当相对误差≤±5%时,干扰物质Z大允许浓度(以μg/mL计)如下:Na+(58),NH4+(16),Al3+(1),Ca2+(0.8),Fe3+(0.8),Mg2+(0.2),Zn2+(0.2),Cu2+(0.1),Cr3+(0.04),NO3-(40),SO42-(40),NO2-(20),SO32-(2),CO32-(2),由以上可知,Na+,NH4+,NO3-,SO42-等允许量较高,一些金属离子如(Cu2+,Cr3+)允许量较小,但雨水中它们的含量不高,并不影响测定。
(三)样品分析
用干净容器收集两份不同时段的雨水,各取3mL的雨水,按照实验方法测定雨水中H2O2的含量,同时做了加标回收,结果见下表。

酶催化分光光度法测定过氧化氢
(一)试验部分
1、仪器与试剂
JASCOV2-530型紫外2可见分光光度计。
过氧化氢标准溶液:用高锰酸钾溶液标定过氧化氢溶液,标准储备溶液0.10mol·L-1,于4℃冰箱内保存,标准工作液浓度为1.0×10-3mol·L-1,现配现用。
血红蛋白(生化试剂)储备液浓度为5.0×10-5mol·L-1,在4℃的冰箱内保存,使用时配成5.0×10-6mol·L-1。
茜素红溶液浓度为1.0×10-3mol·L-1。
氨水2氯化铵缓冲溶液:以氯化铵和浓氨水按不同比例配成pH值分别为9.1,9.5,9.8,10.1,10.4,10.7,11.0的缓冲溶液。
其他试剂均为分析纯,试验用水为二次蒸馏水。
2、试验方法
在10mL比色管中依次加入pH9.8的氨水2氯化铵缓冲溶液2.0mL,1.0×10-3mol·L-1茜素红溶液0.4mL,不同浓度的过氧化氢标准溶液,5.0×10-6mol·L-1血红蛋白溶液2.0mL,用水定容,混合均匀后,室温放置25min。用1cm比色皿于525nm波长处测定吸光度A,以水为参比,同时测定空白溶液的吸光度A0,计算吸光度差值ΔA=A0-A。
(二)结果与讨论
1、反应体系的吸收光谱
按试验方法绘制体系的吸收光谱见下图。从下图中可以看出,有无过氧化氢存在时,体系的吸收光谱峰形相同。即在氨水2氯化铵介质中,空白体系的Z大吸收波长为525nm,加入过氧化氢后,Z大吸收波长不变,但体系的吸光度明显降低,表明在血红蛋白的催化作用下过氧化氢对刚果红具有强烈的氧化能力。
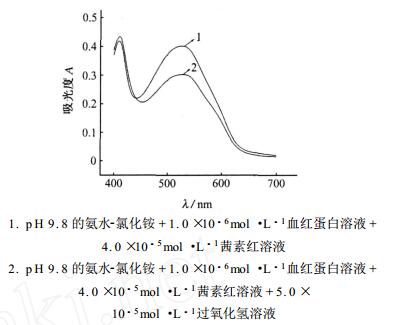
2、试验条件的选择
①介质及酸度
按试验方法对氨水-氯化铵、硫酸、盐酸-邻苯二甲酸氢钾等缓冲体系进行试验,结果表明:在氨水-氯化铵缓冲溶液中,过氧化氢的氧化能力较强,因血红蛋白的催化活性也可被氮配体所增强,并在pH9.8氨水-氯化铵缓冲溶液中ΔA值较大且较稳定。试验选择pH9.8氨水-氯化铵缓冲溶液。
②茜素红溶液用量
试验表明:随茜素红溶液浓度的增大,ΔA值和A值都增大,但茜素红溶液浓度太大,ΔA反而变小。试验选择茜素红溶液的浓度为4.0×10-5mol·L-1。
③血红蛋白用量
试验结果表明:随着血红蛋白溶液用量增大ΔA值增大,但血红蛋白溶液浓度太大,ΔA值反而减小,当血红蛋白溶液的浓度为1.0×10-6mol·L-1时,ΔA值较大,吸光度较稳定,说明此时过氧化氢的氧化能力较强。试验选择血红蛋白溶液的浓度为1.0×10-6mol·L-1。
④反应温度及反应时间
在试验条件下,催化反应在室温即可进行,既减少了酶活性的丧失,又可以避免过氧化氢在高温下分解,并且反应时间达25min后,反应平衡。试验选择25min后进行测定。
3、试剂加入次序对体系吸光度的影响
在pH9.8氨水2氯化铵缓冲溶液中,按不同次序加入茜素红溶液、5.0×10-5mol·L-1过氧化氢溶液、血红蛋白溶液,测定不同加入次序对体系吸光度的影响。试验结果表明:加入次序为缓冲溶液、茜素红、血红蛋白、过氧化氢为Z佳。由于过氧化氢见光易分解,此加入次序能Z大限度发挥过氧化氢的氧化能力。
4、干扰试验
按试验方法对5.0×10-5mol·L-1过氧化氢标准溶液进行测定,当相对误差不超过5%时,以下共存物质不干扰测定:1000倍的NH4+、Na+、F-、HPO42-、草酸,250倍的Cl-、CO32-、乙二胺四乙酸(EDTA)、脲、PO43-,20倍的乳酸,5倍的Cu2+,1倍的Mn2+。对于干扰较大的金属离子,可加入0.1mol·L-1 EDTA溶液掩蔽。
5、标准工作曲线和检出限
按试验方法对过氧化氢标准系列溶液进行测定,以过氧化氢的浓度对其ΔA制作标准工作曲线,过氧化氢浓度在3.0×10-7~8.0×10-5mol·L-1范围内与ΔA呈线性关系,其线性回归方程为ΔA=0.0139+0.0339×105c,相关系数为0.9951,表观摩尔吸光率为1.1×104L·mol-1·cm-1。方法的检出限(3s/k)为5.2×10-8mol·L-1。
6、样品分析
取新鲜雨水,加入0.1mol·L-1 EDTA溶液过滤后,按试验方法进行测定。取不同型号的医用双氧水(主要成分为过氧化氢)2mL,用0.5mol·L-1氯化钾溶液稀释至500mL,按试验方法进行测定,结果见下表。
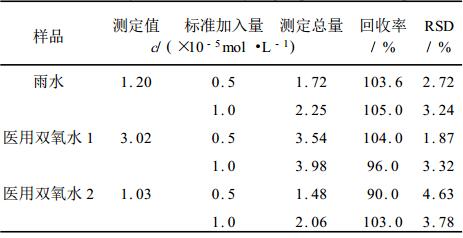
本法将血红蛋白模拟酶作为催化剂,以茜素红为氢供底物显色剂,与其他酶催化体系相比,既减少血红蛋白酶活性的丧失,又避免过氧化氢在高温时的分解。本方法简单、快速、灵敏,室温即可进行催化反应。
①本文由仪器网入驻的作者或注册的会员撰写并发布,观点仅代表作者本人,不代表仪器网立场。若内容侵犯到您的合法权益,请及时告诉,我们立即通知作者,并马上删除。
②凡本网注明"来源:仪器网"的所有作品,版权均属于仪器网,转载时须经本网同意,并请注明仪器网(www.yiqi.com)。
③本网转载并注明来源的作品,目的在于传递更多信息,并不代表本网赞同其观点或证实其内容的真实性,不承担此类作品侵权行为的直接责任及连带责任。其他媒体、网站或个人从本网转载时,必须保留本网注明的作品来源,并自负版权等法律责任。
④若本站内容侵犯到您的合法权益,请及时告诉,我们马上修改或删除。邮箱:hezou_yiqi