盘点国内CAR-T产品的上市历程:科济CAR-T再领创新风潮!
CAR-T研发历程
国产CAR-T药物的研发历程可谓波澜壮阔。从Z初的科研探索,到临床试验的开展,再到Z终的上市批准,每一步都凝聚了众多科研人员的智慧和汗水。
2021年,初露锋芒,复星凯特的阿基仑赛注射液和药明巨诺的瑞基奥仑赛注射液成为中国首批获得药品监督管理局受理上市申请的CAR-T细胞药品。这标志着中国CAR-T疗法的正式起步,为后续产品的开发和上市奠定了基础。
随后几年,国内CAR-T产品的研发和上市进入了井喷期。2023年中国首款BCMA CAR-T南京驯鹿的伊基奥仑赛注射液获批上市。同年,合源生物的纳基奥仑赛注射液获得中国国家药监局的上市批准,用于治疗成人复发或难治性B细胞急性淋巴细胞白血病 (r/rB-ALL) ,成为首款在中国获批上市的治疗白血病的CAR-T产品。
图1:全球细胞治疗CAR-T上市产品盘点
国产CAR-T药物崭露头角
2024年3月1日,科济药业,一家主要专注于治疗血液恶性肿瘤和实体瘤的创新CAR-T细胞疗法公司宣布,国家药品监督管理局已经正式批准赛恺泽(泽沃基奥仑赛注射液,产品编号:CT053,一种针对BCMA的自体CAR-T候选产品)的新药上市申请,用于治疗复发或难治性多发性骨髓瘤成人患者。
图2:科济赛恺泽(泽沃基奥仑赛注射液)获批上市
上下滑动查看更多
CAR-T药物有望惠及更多患者
随着技术的不断进步和临床应用的不断拓展,CAR-T药物有望在更多的领域发挥重要的作用,为患者带来福音。
药明巨诺的倍诺达此前已在国内获批两个适应症,即用于治疗经过二线或以上系统性治疗后成人患者的r/r大B细胞淋巴瘤 (LBCL) ,以及于治疗复发或难治性滤泡淋巴瘤 (r/rFL) 患者。今年1月,药明巨诺宣布瑞基奥仑赛针对复发或难治套细胞淋巴瘤患者的新适应症上市许可申请已获得国家药监局受理。去年4月,瑞基奥仑赛用于治疗中重度难治性系统性红斑狼疮的临床试验申请也已获得批准。
科济药业旗下的泽沃基奥仑赛注射液S发价格为115万元,预计该药的年终端销售额的峰值可达10亿元以上。同时,公司会积极帮助患者获得惠民保和商业保险等支持,希望未来能有更多多元化支付方式提高CAR-T治疗的可及性。我们有理由相信,在未来的日子里,中国CAR-T药物将继续书写新的辉煌篇章,为人类的健康事业做出更大的贡献。
助力细胞治疗研发
作为细胞治疗的先驱者,自2017年第一款细胞治疗药物开始,一次又一次助力细胞治疗药物产品的研发、转化、上市与生产。
采用波浪式生物反应器进行免疫细胞(如T细胞,NK细胞等)的制备,不仅可以灵活实现不同培养体积的切换 (300 mL-25 L) 。同时通过在封闭的细胞培养袋中进行自动的补液培养或不同的灌流策略可以收获高密度、高活性的细胞产品。
图3:Xuri W25细胞扩增系统
在细胞的分离、病毒转导、清洗、分装等过程中,可应用Sepax C-pro多功能细胞处理系统,实现密闭式、自动化的全流程控制。
图4:Sepax C-pro自动细胞处理系统
VIA Thaw L1000干热式细胞复苏仪,专为细胞冻存袋解冻而设计,除了常规的细胞系外,也适用于T细胞、NK细胞等各类治疗性细胞的冻存。可以兼容市场上主流的1 L及以下冻存袋,体积容量在10 mL到275 mL之间,盖子上配备四个按摩头及五个红外温度感应器,可对整个细胞复苏流程进行监控。
图5:VIA Thaw L1000干热式细胞复苏仪
创新促发展,细胞治疗新品加速细胞治疗研发与商业化,3月15日 E馆 E301 13:00,与您不见不散!
声明:本文为作者原创S发,严禁私自转发或抄袭,如需转载请联系并注明转载来源,否则将追究法律责任
点亮
与
,传递信息 ↓ ↓
全部评论(0条)
推荐阅读
-
- 盘点国内CAR-T产品的上市历程:科济CAR-T再领创新风潮!
- 文末扫码进入云展台,精彩活动提前掌握!
-
- 赛默飞CTS产品助力合源生物CAR-T治疗产品源瑞达在国内获批上市!
- 赛默飞CTS产品助力合源生物CAR-T治疗产品源瑞达在国内获批上市!
-
- 千呼万唤,传奇生物CAR-T产品中国获批!
- 文末扫码了解Sefia细胞制备平台应用数据
-

- 赛科成摆床反应器助力CAR-T细胞治疗产品规模化扩增
- 细胞治疗是对肿瘤患者或健康供者来源的免疫细胞于体外进行基因改造,赋予其肿瘤靶向性识别和杀伤能力,经体外扩增后将其回输患者体内,对肿瘤发起精zhun、高效的攻击,并可激活自身免疫系统对肿瘤的免疫应答。
-
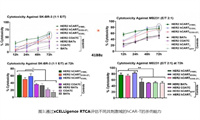
- “CAR-T之父”Carl June合作团队开发新型癌症免疫疗法:“headless” CAR-T
- 总之,该临床前研究表明 hCART41BBζ杀伤作用明显,联合不同BATs在持续和连续性杀伤试验中杀死肿瘤靶点,分泌 Th1 细胞因子和趋化因子,并在体外缺氧条件下表现出特异性靶向杀伤。
-

- 1月CAR-T行业十大热点
- 从2017年诺华和Kite的两款CAR-T产品上市之后,国内外的CAR-T细胞在研疗法几乎是爆发式增长。2020年,国内迎来首个CAR-T细胞治疗产品的上市申请受理。自此,中国CAR-T市场正式进入商业化阶段。
-

- CAR-T细胞载体拷贝数检测的qPCR法考量
- CAR-T和TCR-T都属于比较主流的特异性免疫细胞治疗,且细胞来源相同,均来自外周血单核细胞(PBMC)、自体或同种异体细胞。
-

- 复制型慢病毒RCL检测Kit助力CAR-T产品质控放行
- 大多数应用于细胞基因治疗的逆转录病毒和慢病毒均被设计为复制缺陷型病毒载体。对于复制缺陷型病毒载体,在生产中可能发生经缺失改造的载体与野生型病毒序列之间的同源重组,导致产生复制型病毒。终产品中复制型病毒的存在有可能引起病人不良反应,构成临床隐患和潜在危险,甚至引发肿瘤,故对复制型病毒检测是安全性检测中非常重要的项目。
-

- CAR-T细胞治 疗产品指导原则又有变更?事关从业者,速看!
- 6 月 26 日,国家药品监督管理局药品审评中心发布了《自体 CAR-T 细胞治 疗产品药学变更研究问题与解答(征求意见稿)》,用于规范和指导 CAR-T 类产品的变更研究和申报。
-
- 百年细胞治疗史,CAR-T未来如何突破?
- 作为免疫治 疗产品,CAR-T 存在免疫相关一些副作用,包括细胞因子风暴(CRS)和神经毒性等,如上表统计 6 已经上市产品[5-7]。此外,脱靶毒性等也是不能忽略的问题。
-

- 自体CAR-T细胞药品供应链管理规范开始实施
- 10月13日,全国团体信息平台发布了由上海医药行业协会和上海药品审评核查中心组织起草的《自体CAR-T细胞药品供应链管理规范》(T/SHPPA 011—2021)团体标准,该标准2021年10月18日起实施。
-
- 一文了解CAR-T细胞疗法新进展:提升有效性与安全性的策略
- 有望进一步提高CAR-T疗法的有效性和安全性,使其成为更多癌症患者可行的治疗选择。
-

- CAR-T细胞再次全新升级,或将根除致命实体瘤
- 为了建立增殖基因开关,研究人员使用TMX诱导型synZiFTR来调节超级IL-2的表达,有效地在体内和体外对治疗相关基因进行剂量和时间依赖性控制。
①本文由仪器网入驻的作者或注册的会员撰写并发布,观点仅代表作者本人,不代表仪器网立场。若内容侵犯到您的合法权益,请及时告诉,我们立即通知作者,并马上删除。
②凡本网注明"来源:仪器网"的所有作品,版权均属于仪器网,转载时须经本网同意,并请注明仪器网(www.yiqi.com)。
③本网转载并注明来源的作品,目的在于传递更多信息,并不代表本网赞同其观点或证实其内容的真实性,不承担此类作品侵权行为的直接责任及连带责任。其他媒体、网站或个人从本网转载时,必须保留本网注明的作品来源,并自负版权等法律责任。
④若本站内容侵犯到您的合法权益,请及时告诉,我们马上修改或删除。邮箱:hezou_yiqi




















参与评论
登录后参与评论