可靠 | 稳定 | 高效 | 创新
享受丝滑生活
荧光猝灭体(Quenchbodies)是一种在与抗原结合时荧光强度会增强的荧光标记抗体,在生物传感器开发方面展现出巨大潜力。基于纳米抗体的荧光猝灭体因其体积小、易于表达、稳定性高、进化速度快以及易于蛋白质工程改造等特点而格外引人注目。然而,现有的蛋白质检测设计动态范围有限,荧光强度仅增加 1.1 至 1.4 倍。在此,我们确定了纳米抗体互补决定区(complementarity-determining regions,CDR)中对荧光猝灭体性能至关重要的色氨酸残基。通过合理设计与分子动力学模拟相结合的方法,我们开发出一种优化的纳米抗体支架,并在关键位置引入色氨酸。我们利用该支架在体外针对人类炎症细胞因子白细胞介素 -6(IL-6)进行了定向进化筛选。这产生了荧光强度增加 1.5 至 2.4 倍的荧光猝灭体,能够检测低至 1 至 2 nM的 IL-6。我们的支架为开发针对各种蛋白质靶点的生物传感器提供了有价值的平台,适用于研究、诊断和环境监测等领域。
疾病生物标志物的检测在现代医学的各个方面都至关重要。蛋白质检测尤为重要,因为与基因标志物相比,蛋白质的存在往往直接与疾病表型相关。分析型质谱法是研究蛋白质组和鉴定蛋白质生物标志物的金标准。然而,质谱法通常需要大型且昂贵的设备,并且检测过程冗长复杂。相比之下,免疫测定法使用简便、快速、选择性强、灵敏度高且价格实惠。这些特点使得免疫测定法在临床环境中备受关注,因为快速诊断有助于早期治疗和预防传染病的传播。
免疫测定法利用抗体检测抗原。免疫测定法的读出结果可基于多种输出信号,包括酶反应监测、荧光、化学发光和色谱分离。无论其输出信号如何,免疫测定法通常可分为异相和均相两类。在异相测定法中,抗体结合的抗原需要与未结合的抗体和抗原分离。酶联免疫吸附测定(ELISA)是一种著名的异相免疫测定法,依赖于酶输出,常用于研究和临床环境。侧向流动测定法是另一种常见的异相免疫测定法,近年来在即时检测环境中越来越受欢迎,因其速度快且易于使用。然而,异相免疫测定法通常需要较长的孵育时间和大量的洗涤步骤,使得分析物检测既费力又耗时。相比之下,均相“混合即读”免疫测定法无需分离步骤,因此更快、更简单。AlphaLISA是均相酶联免疫吸附测定(ELISA)式免疫测定的一个实例,旨在克服传统 ELISA 所涉及的繁琐程序。所有这些测定都需要一对经过表征的抗体,能够同时在抗原的两个不同表位上结合,这被认为是所有夹心式免疫测定开发中的主要瓶颈。这些问题可以通过使用一种荧光标记的抗体(称为“淬灭体”)来解决。
淬灭体及其工作原理已在其他地方详细论述。简而言之,淬灭体通常是单链可变区(scFv;32 千道尔顿)或抗体的抗原结合片段(Fab;50 千道尔顿),通过一个柔性肽连接子与荧光团相连。这种柔性连接子使得荧光团能够与淬灭体中的色氨酸残基相互作用。这种相互作用会导致荧光偏振(1/r)发生微小变化,但通过光诱导电子转移,荧光强度会更显著地降低(图 1A)。只要荧光团与淬灭色氨酸的距离在≤10 埃以内,疏水/π–π 堆积相互作用就会促进电子转移。当淬灭体与其特异性抗原结合时,由于空间位阻阻碍了荧光团与色氨酸的相互作用,淬灭的荧光团荧光强度会增加(图 1A)。淬灭体与抗原结合时荧光强度的增加可用于均相免疫测定,从而快速测量抗原浓度,甚至在复杂生物样本(如人血浆)中也是如此。
图 1:从头设计的淬灭体的设计与计算机模拟建模。
A 为淬灭体工作原理的示意图。在无抗原的情况下(左),荧光团被抗体中的色氨酸淬灭。在抗原结合状态下(右),荧光团被移位,导致去淬灭并使荧光强度增加。B 以 PDB ID: 5M14 为模型的 MBP 结合淬灭体(蓝色)的拟议机制,其 N 端共价连接的荧光团(绿色)因与基于 CDR 的色氨酸(红色球体)相互作用而发生淬灭。与 MBP 抗原(灰色表面模型)结合后,荧光团因被色氨酸(W101、W110 和 W115)遮挡而不再淬灭,这与荧光强度增加有关。C 通过分子动力学模拟得出的在无(蓝色)或有(绿色)抗原存在时 MBP 结合纳米体中荧光团与三个色氨酸(W101、W110 和 W115)中任一的距离的平均归一化分布直方图。当距离≤10? 时,荧光团被认为被色氨酸淬灭(阴影区)。W101、W110 和 W115 的单独图谱见图 S1A。图中展示了在没有抗原(蓝色)或存在抗原(绿色)的情况下,通过分子动力学模拟得到的荧光团与两个色氨酸(W103 和 W115)中任一个的距离的平均归一化分布直方图。W103 和 W115 的单独分布图见图 S1B。
目前大多数淬灭体基于单链可变片段(scFv)和抗体片段(Fab),但基于骆驼科动物来源的单域纳米抗体的淬灭体却很少,尽管纳米抗体具有几个关键优势。这些优势包括体积小(约 15 千道尔顿)、易于表达、稳定性高、可进化以及适合蛋白质工程改造。动物来源的抗体生产涉及漫长的周期和批次间的一致性问题。相比之下,计算模型和合成纳米抗体生产的进步为快速开发能识别广泛目标的淬灭体开辟了道路。基于纳米抗体的淬灭体特别适合识别像小分子药物或肽这样的较小抗原,当淬灭体与甲氨蝶呤结合时,观察到的最大荧光强度增加可达 6 倍。然而,对于较大的蛋白质抗原,识别效果通常较差,对于白蛋白、闭合蛋白、人表皮生长因子受体 -2 和血凝素,荧光强度增加仅为 1.1 至 1.4 倍,这可能是由于这些抗原中的氨基酸导致了额外的淬灭作用。关键纳米抗体色氨酸相对于荧光团的位置优化可能会提高基于纳米抗体的淬灭体的性能。
因此,我们试图构建一种通用的含色氨酸的纳米抗体基淬灭体支架,色氨酸位于最佳位置,从而能够以更出色的性能识别蛋白质抗原。我们选择通过淬灭体 N 端的半胱氨酸标签直接连接 TAMRA,因为在之前的研究中,该研究对多种纳米抗体基淬灭体的连接子长度和荧光团进行了筛选,发现这种方式能产生最高的响应。对代表性的溶菌酶结合纳米抗体和麦芽糖结合蛋白(MBP)结合纳米抗体进行结构机制的计算机模拟,揭示了内在色氨酸位置的重要性。然后对这些淬灭体进行理性诱变以提高荧光团的淬灭效果。由此产生的高性能淬灭体支架被用作体外定向进化筛选针对白细胞介素 -6(IL-6)的基础。该筛选产生了一种纳米抗体基淬灭体,在检测 IL-6 时荧光强度提高了 2.4 倍。我们的高性能纳米抗体基淬灭体是一种通用支架,适用于生产用于检测各种临床蛋白质抗原的荧光生物传感器。
图 2:抗原结合时淬灭体的荧光强度变化。
将 A 型麦芽糖结合蛋白(MBP)或(B)溶菌酶淬灭体在不断增加浓度的其相应抗原存在下(25°C,60 分钟)进行孵育。数据为相对于 0 nM 抗原天然样本的荧光倍增平均值±标准差(激发波长 = 535 ± 20 纳米,发射波长 = 585 ± 30 纳米)。统计学上显著检测的最低点已标出(普通单向方差分析,Tukey 多重比较,p = 0.002),虚线左侧所列浓度视为无显著性(α = 0.05)。(C)MBP 或(D)溶菌酶淬灭体对其相应抗原的荧光强度响应进行了量化,并拟合到描述单个位点特异性结合模式的方程中,以推导出半最大效应浓度(EC50)作为淬灭体结合亲和力(KD)的替代测量值。数据为平均值±标准差的归一化荧光强度。
图 3:溶菌酶和麦芽糖结合蛋白淬灭体中的色氨酸介导的淬灭。
A 图为基于 PDB 编号 1ZVH 的溶菌酶淬灭体(蓝色)模型,突出了所有内源性酪氨酸(黄色棒状)和色氨酸(红色球体,如标注),与溶菌酶(灰色表面模型)形成复合物。B 图为野生型、W103Y、W115Y 和 W103Y/W115Y 溶菌酶淬灭体变体在 500 nM 溶菌酶存在下的折叠感知。C 图为野生型、Y27W、Y104W、Y110W、单突变体、双突变体和三突变体溶菌酶淬灭体变体的折叠感知。D 图为基于 PDB 编号 5M14 的麦芽糖结合蛋白淬灭体(蓝色)模型,突出了所有内源性酪氨酸(黄色棒状)和色氨酸(红色球体,如标注),与麦芽糖结合蛋白(灰色表面模型)形成复合物。E 图为野生型与 W101A/W110A/W115A 三突变体在 500 nM 麦芽糖结合蛋白存在下的折叠感知。F 图为野生型、Y33W、Y54W、Y59W 和 Y114W、双突变体、三突变体和四突变体麦芽糖结合蛋白淬灭体变体的折叠感知。数据为平均值±标准差(激发波长 = 535 ± 20 纳米,发射波长 = 585 ± 30 纳米)。采用普通单向方差分析结合 Tukey 多重比较检验,显示显著(**** = p < 0.0001)或不显著(ns)差异。
图 4:用于结合白细胞介素 - 6 的新型 CDR 色氨酸猝灭体的进化。
A 我们优化色氨酸的纳米抗体支架模型。B 定向进化工作流程示意图。(i)由变体基因(蓝色)与 SNAP 基因(灰色)相连的基因文库被组装并连接到与苯基鸟嘌呤部分(BG)相连的树状 DNA 共轭物上。(ii)基因构建体被封装在含有无细胞表达试剂的单个微滴中。表达的 SNAP 标签变体与基因构建体结合,从而实现表型与基因型的关联。(iii)对变体进行筛选和测序,以测量每个变体的读取数。线条显示了第 1 至 5 轮的标准化读取数,通过 2 次技术重复选择对 IL-6 的结合。每个命中变体以单独的颜色表示。C 在不断增加的 IL-6 浓度下,淬灭体变体 #1 的倍数变化。D 在不断增加的 IL-6 浓度下,淬灭体变体 #10 的倍数变化。统计学上显著检测的最低点被标出(普通单向方差分析,Tukey 多重比较,p < 0.0001),虚线左侧列出的浓度被认为不显著(α = 0.05)。E 在不断增加的 IL-6 浓度存在下,亲和力成熟的淬灭体变体 #15 的折叠感应显示 EC50 = 20 nM,并且能显著检测到低至 1 nM 的浓度。F 在不断增加的 IL-6 浓度存在下,亲和力成熟的淬灭体变体 #35 的折叠感应显示折叠感应为 2.4,并且能显著检测到低至 2 nM 的浓度。
淬灭体的 DNA 和蛋白质序列设计
从结合麦芽糖结合蛋白的纳米抗体或结合溶菌酶的纳米抗体中提取的蛋白质编码序列,设计时加入了(i)一个 N 端半胱氨酸标签,作为荧光标记的目标;(ii)一个 C 端 Avi 标签,以实现生物素化;(iii)一个 3× FLAG 标签和 10× His 标签,以方便纯化过程。随后,整个蛋白质编码元件被转换为 DNA,并使用 IDT 的大肠杆菌(E. coli)B 菌株优化器进行了密码子优化。此蛋白质编码 DNA 元件随后被整合到一个基因表达盒中,该盒带有 T7 启动子和终止子,用于无细胞体外转录和翻译(IVTT)蛋白质产物,并从 IDT 订购为 Geneblock。该 Geneblock 还带有适合聚合酶链式反应(PCR)复制 Geneblock 的侧翼 DNA 元件,具体为与正向引物 5′-ACCCGGCATGACAGGAG-3′ 和反向引物 5′-TGGCGGCCGCTCTA-3′ 相互补的 DNA。Geneblock 的 PCR 复制使用 Q5? Hot Start 高保真酶混合物(NEB;以 100 微升的规模进行操作,使用 50 纳克的基因块作为模板,以及 0.5 微摩尔的正向和反向引物,在 PCR Mastercycler中进行反应,先在 98 摄氏度下加热 30 秒,然后进行 32 个循环,每个循环包括变性(98 摄氏度,10 秒)、退火(60 摄氏度,30 秒)和延伸(72 摄氏度,15 秒)。使用 Wizard Clean-up 套件(Promega)对淬灭体 PCR 产物进行纯化,并在 Nanodrop 2000C 分光光度计上通过 A260/A280 吸光度测定进行定量。在用于体外转录翻译(IVTT)之前,通过琼脂糖凝胶电泳进一步分析淬灭体 PCR 产物,以确保 PCR 产物的大小和纯度符合预期。所有突变型淬灭体都是通过在计算机上对 5M14 和 1ZVH 淬灭体构建体的序列进行修改,并从 IDT 重新订购为基因块而生成的。
体外淬灭体表达、标记和纯化
对于每个淬灭体,将 600 ng 的纯化 PCR 产物与 NEBExpress? 无细胞大肠杆菌蛋白质合成系统(NEB)按 2 倍反应规模混合,包括蛋白质二硫键增强剂(NEB)和 GamS(NEB),按照制造商的说明进行操作,并在室温下以 1200 rpm 的转速在 Thermomixer(Eppendorf;用于所有后续的振荡和孵育步骤)中振荡孵育 16 小时。然后将表达的淬灭体从粗 IVTT 混合物(100 μL)中纯化,方法是将其与 12.5 μL 的 Pierce Anti-DYKD4K(FLAG)磁性琼脂糖珠(相当于 50 μL 的原始悬浮液)混合,该磁珠预先用磷酸盐缓冲盐水(PBS)洗涤,使用 MagJET 分离磁铁(用于所有后续的洗涤步骤)。将粗 IVTT-FLAG 珠混合物在室温下振荡 30 分钟,1200 rpm,以使带有 FLAG 标签的淬灭体与磁珠结合,随后用 0.2 mL PBS 洗涤。对于结合 MBP 的淬灭体,磁珠还需用 0.2 mL 溶于 PBS 的 0.5 M 麦芽糖洗涤一次,以去除内源性 MBP(作为污染物存在于内源性大肠杆菌无细胞裂解液中),因为麦芽糖会与纳米体竞争结合 MBP。随后,用 100 微升含 1 毫摩尔/升三(2-羧乙基)磷(TCEP)的 PBS 洗涤珠子 10 分钟,温度为 16 摄氏度,转速为 1200 转/分钟,接着用 0.2 毫升脱气 PBS 再次洗涤。然后立即将珠子与 100 微升浓度为 250 微摩尔/升的带有 C6 连接臂的 5(6)-羧基四甲基罗丹明(TAMRA)马来酰亚胺(溶解于含 1%(体积比)二甲基亚砜(DMSO)的脱气 PBS 中)混合,在室温下以 1200 转/分钟的速度孵育 3 小时。然后用 9 次 0.2 毫升的 PBS 洗涤珠子,以去除未结合的染料。最后,用 50 微升 1.5 毫克/毫升的 Pierce? 3×DYKDDDDK 肽(ThermoFisher)从珠子上洗脱淬灭体。
十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)和凝胶内荧光分析
蛋白质在 2× 变性 Tris-甘氨酸样品缓冲液中稀释至最终浓度为 63 mM Tris-HCl、10%(体积比)甘油、5%(体积比)β-巯基乙醇、2%(质量比)十二烷基硫酸钠(SDS)、0.0025%(质量比)溴酚蓝,pH 6.8,然后在 Tetra 电泳系统中使用 Mini-PROTEAN TGX 预制凝胶进行 150 V 电压下 30 分钟的 SDS-聚丙烯酰胺凝胶电泳(SDS-PAGE),电泳缓冲液为 Tris-甘氨酸运行缓冲液(25 mM Tris、192 mM 甘氨酸、0.1%(体积比)SDS,pH 8.3),操作依照制造商的说明。使用 Precision Plus 双色蛋白质标准品估算蛋白质大小。所有凝胶均用 Instant Blue染色过夜,随后在 MilliQ H2O 中脱色过夜,然后在 Gel Doc XR+ 分子成像仪上成像。SDS-PAGE 后凝胶内淬灭体的 TAMRA 荧光在 Amersham Typhoon 生物分子成像仪(Cytiva)上进行分析,使用预设的 Cy3 成像采集设置(激发波长 = 532 nm,发射滤光片 = 570 ± 20 nm)。
下拉结合试验
为评估其抗原结合能力,按照上述方法表达淬灭体,并从 100 μL 粗 IVTT 混合物中通过与 12.5 μL 磁珠/50 μL Pierce Anti-DYKD4K(FLAG)磁性琼脂糖悬浮液(30 分钟,1200 转/分钟)结合来纯化淬灭体。然后将粗 IVTT-FLAG 磁珠混合物在室温下以 1200 转/分钟的速度混合 30 分钟,使带有 FLAG 标签的淬灭体与磁珠结合,随后加入 100 μL 的(i)1 μM 的麦芽糖结合蛋白(MBP)用于 MBP 结合淬灭体,或(ii)10 μM 的溶菌酶用于溶菌酶结合淬灭体,并在室温下以 1200 转/分钟的速度孵育 30 分钟。接着用 6×0.2 mL 的 PBS 洗涤磁珠以去除任何未结合或非特异性结合的抗原,最后用 50 μL 的 1.5 mg/mL Pierce? 3× DYKDDDDK 肽进行洗脱。通过 FLAG 下拉获得的洗脱淬灭体 - 抗原复合物进行还原 SDS-PAGE 分析,并通过与野生型(WT)对照的结合情况半定量分析突变对抗原结合的影响。
蛋白质:TAMRA 定量
通过在 Nanodrop 2000C 分光光度计上测量 A280 吸光度来定量 TAMRA 标记的淬灭体的蛋白质浓度,并以 PBS 中的 FLAG 肽标准品为参照进行校正,该标准品经过相同的洗脱程序以校正与 FLAG 肽相关的背景吸光度。蛋白质浓度进一步通过纳入 TAMRA 的校正因子(A280 = 0.178)并假设基于 ExPaSy ProtParam67 计算的多肽序列特性得出的消光系数(淬灭体的 ε 约为 47,000 cm?1 M?1)来计算。TAMRA 标记的淬灭体中 TAMRA 的浓度通过进一步测量 A555 并假设 TAMRA 的消光系数为 90,000 cm?1 M?1 来确定。
荧光分光光度板式测定法
淬灭体在不含或含 8000、4000、2000、1000、500、250、125、64、32、16、8、4、2 或 1 nM 配体抗原(溶菌酶、麦芽糖结合蛋白或白细胞介素 -6)的 PBS/0.05%(体积比)吐温 -20(PBST)中稀释至 20 nM,或在含 2%(质量比)十二烷基硫酸钠和 5%(体积比)β-巯基乙醇作为变性剂的溶液中,于室温下孵育 1 小时。随后将样品(n = 3,每孔 40 μL)分配到黑色 384 孔 Greiner 微孔板中,并在 CLARIOstar 微孔板读数仪中通过荧光分光光度法进行分析,激发波长为 535 ± 20 nm,发射波长为 585 ± 30 nm,使用 557.5 nm 的二向色性滤光片。为了比较在不同浓度抗原存在时的荧光增加情况(“倍数感应”),将所有原始荧光值归一化为不含任何抗原或变性剂的 0 nM 淬灭体对照的比率。为了得出淬灭体的结合亲和力,从所有含抗原的样品中减去 0 nM 抗原的淬灭体荧光信号,并在 GraphPad Prism 9.4.0 中将数据拟合到描述单个位点特异性结合模式的方程(含希尔斜率),以得出平衡解离常数(KD)。WT Qb-MBP 在三个不同的时间点进行了表达和测试,包括各重复实验之间的时间间隔,结果显示各重复实验的结果基本一致,这表明在研究本研究中的其他任何突变体时,生物学重复实验是多余的。
淬体库装配
如先前所述,使用经三聚体磷酰胺酯混合物(TRIM)随机化的寡核苷酸构建了具有可进化的互补决定区(CDR)的噬菌体展示文库,但做了以下修改。使用Vent聚合酶(NEB)通过PCR组装构建了CDR 1 - 3,每个反应包含1× ThermoPol缓冲液、5%(v/v)二甲基亚砜(DMSO)、脱氧核苷三磷酸(dNTPs)(0.4 mM)、正向和反向外引物(1 μM)、随机TRIM寡核苷酸(50 nM)、大引物(25 nM)、组装引物(25 nM)和Vent聚合酶(2 U),最终反应体积为100 μL。大引物以4 nmol超长寡核苷酸(IDT)形式购买。随机TRIM寡核苷酸从IDT或Ella Biotech GmbH购买。CDR 1 反应包含CDR1_c随机TRIM寡核苷酸、megaprimer1_c、FW2_C_rev组装引物和FW1_c_for及Link1_c_rev外引物。CDR2 反应包含Q_CDR2_c随机化寡核苷酸、megaprimer2_c以及Link1_c_for和Link2_c_rev外引物。CDR3 反应包含Q_CDR3_c随机化寡核苷酸以及Link2_c_for和FW4_c_rev外引物。PCR组装反应条件为:94°C初始变性2分钟,然后进行30个循环,每个循环94°C 30秒、60°C 30秒、72°C 30秒,最后在72°C延伸5分钟。单个反应在 Macherey-Nagel 凝胶纯化柱上进行纯化。编码 CDR1 和 CDR2 的 DNA 片段分别用 BsaI-HFv2 和 BbsI-HFv2 酶过夜消化(NEB)。反应产物用 Macherey-Nagel 凝胶纯化柱进行纯化。对 DNA 产物进行定量,并以等摩尔混合物进行连接。正确连接产物经凝胶提取后,用外侧引物 FW1_c_for 和 Link2_c_rev 进行 PCR 扩增。CDR1 + 2 片段用 BsaI-HFv2 消化,CDR3 片段用 BbsI-HFv2 消化,并用 T4 连接酶连接。正确连接产物经凝胶提取。通过 8 个循环的 PCR 在组装好的文库末端添加 BbsI 限制性位点。PCR 产物随后用 BbsI 消化,并用 T4 连接酶连接到表达载体上。
SNAP 显示选择
编码纳米抗体变体的基因通过甘氨酸/丝氨酸连接序列与 SNAP 标签的 N 端相融合,作为在 T7 启动子控制下的表达盒的一部分。基因被融合到类似树枝状的 DNA 结构(DL-DNA)上,使得每个基因都展示出八个苯甲基鸟嘌呤基团,如先前所述。为了组装纳米抗体文库表达盒,我们将 50 ng 经 BbsI 酶切的纳米抗体文库与 200 ng 经 BbsI 酶切的表达载体在 16°C 下反应 1 小时,载体带有互补的突出端。随后,用含有尿嘧啶和与热不稳定 USER II 酶切/连接兼容的突出端的“outPCR”引物对连接产物进行扩增(NEB)。outPCR 后,通过同时进行热不稳定 USER II 酶切和 T4 连接,将 DL-DNA 组装到具有兼容粘性末端的 DL-DNA 结构上。通过琼脂糖凝胶电泳确认连接产物。将基因稀释至 125 pM,在 30 μL PURExpress 无细胞表达混合物(NEB)中,该混合物含有 0.06% 的泊洛沙姆 F-127(最终浓度)以及每种 1 μL 的二硫键增强剂 1 和 2(NEB #E6820)。我们使用了由 3M? Novec? HFE7500 工程流体(3M)制成的液滴油,该油经过 2 微米纤维素过滤器(VWR)过滤,并添加了 2% 的氟化表面活性剂 FluoSurf 纯品(Emulseo,#1903)用于液滴乳化。乳化时,将 0.4 毫升液滴油装入 1 毫升鲁尔锁注射器中,然后将无细胞表达混合物置于其上。将装有 0.8 毫升液滴油的 1 毫升注射器连接到由 Shirasu 多孔玻璃(SPG)提供的 5 微米疏水膜泵送装置(#PC05U)。将油相通过 SPG 膜推挤,直至油相与开口端齐平。然后将装有无细胞表达混合物的注射器连接到 SPG 膜上,并通过反复将混合物在两个注射器之间交替,总共快速挤出 10 次,完成乳化过程。乳化过程产生体积在飞升范围内的单分散液滴。在 PURExpress 无细胞表达混合物中浓度约为 125 皮摩尔时,液滴装载量为每液滴 0.1 个基因。随后将乳液转移至新的 1.5 毫升管中,在 37 摄氏度下孵育 4 小时,然后在 4 摄氏度下于 Eppendorf 恒温振荡器中过夜。为破乳,用 23 号针头从管底吸出多余的 HFE 油,然后向管中加入与乳液体积 1:1 的全氟辛醇(西格玛奥德里奇/默克,#370533)。涡旋 15 秒后,将管以 13000 转/分钟离心 1 分钟,将水相转移至干净的管中。回收的乳液用 5 倍的回收和结合缓冲液(RBB;40 毫摩尔/升 Tris-HCl,pH 7.4,10 毫摩尔/升 EDTA,1 毫摩尔/升二硫苏糖醇,0.5%吐温-20 和 10 微摩尔/升 BG-mPEG12)稀释。通过用 1 毫升 PBS 洗涤 70 微升对甲苯磺酰基活化的 M-280 磁性 Dynabeads(赛默飞世尔 #14203),3 次,每次 5 分钟,制备显示重组 IL-6 蛋白的磁珠(BioLegend #570806)。将 10 微克的 IL-6 用 PBS 稀释至 75 微升,制备 IL-6 结合缓冲液。将磁珠与 70 微升的 IL-6 结合缓冲液在 37 摄氏度下端对端混合过夜偶联。通过在纳米滴定仪上于 280 纳米处测定结合前和结合后溶液的吸光度,确定了与磁珠结合的 IL-6 的量。结合后,磁珠用 1 毫升 PBS 洗涤 1 次,然后用 1 毫升 50 毫摩尔/升 Tris-HCl(pH 7.5)、0.5%吐温 -20 洗涤 1 小时,期间不断翻转混合。最后,磁珠在 1 毫升 PBS 中洗涤 1 小时,再洗涤 1 次,并在 20 微升 50 毫摩尔/升 Tris-HCl(pH 7.5)、0.5%吐温 -20 中重悬。随后,通过在涂有 IL-6 的磁珠(除非另有说明,IL-6 浓度为 500 纳摩尔当量)上进行亲和淘选,选择 SNAP 显示复合物,总反应体积为 75 微升(保留 2 微升溶液用于 qPCR 分析),在室温下翻转混合 1 小时。淘选后,用 200 微升 RBB 洗涤 5 次。然后通过热休克(70 摄氏度 20 分钟)在 15 微升 50 毫摩尔/升 Tris-HCl(pH 7.5)、0.5%吐温 -20 中释放结合的复合物,并使用 Q5? 热启动聚合酶(NEB)和正向引物:GATCACGAAGACATTATGGCGGATCAAGTCCAGCTGGTGGAATCG 以及反向引物:GATCACGAAGACATCACCAGAACGGTAACTTGGGTGCCCTG 对所选基因进行 PCR 扩增。PCR 反应由 10 微升 Q5 反应缓冲液(NEB)、1 微升 10 毫摩尔脱氧核苷三磷酸(NEB)、各 2 微升 10 微摩尔的正向和反向引物、5 微升洗脱液、24.5 微升无核酸酶水、5 微升二甲基亚砜和 0.5 微升热启动 Q5 高保真聚合酶组成。循环条件为 98 摄氏度 2 分钟,接着进行 25 至 30 个循环,每个循环 98 摄氏度 30 秒、60 摄氏度 20 秒和 72 摄氏度 30 秒,最后在 72 摄氏度延伸 2 分钟。通过琼脂糖凝胶电泳验证回收基因的扩增情况。所选基因随后可重新格式化以进行进一步的选择轮次。
统计学与可重复性
使用 GraphPad Prism 9.4.0 进行了统计分析。结合曲线拟合到具有希尔斜率的单个位点特异性结合模型,以得出平衡解离常数。荧光分光光度板检测实验在每种条件下进行了三次技术重复,数据以平均值±标准差(SD)的形式报告。对于针对麦芽糖结合蛋白(MBP)的淬灭体(Qb-MBP),实验在三个不同时间间隔独立重复进行,结果基本相同。分子动力学模拟对每个系统进行了六次独立重复,apo 状态总计 72 微秒,抗原结合状态总计 36 微秒。对于体外进化实验,进行了两次 NGS 选择的技术重复,并在五轮选择中评估了富集情况。在进行统计学显著性检验(例如 IL-6 滴定)时,使用了一向方差分析(ANOVA)结合 Tukey 多重比较法,显著性水平定义为α = 0.05。
参考文献:
Cater, J.H., El Salamouni, N.S., Mansour, G.H. et al. Optimised nanobody-based quenchbodies for enhanced protein detection. Commun Biol 8, 937 (2025). https://doi.org/10.1038/s42003-025-08359-3
扫描关注微信公众号,随时了解更新信息!
扫描关注,随时沟通。
全部评论(0条)
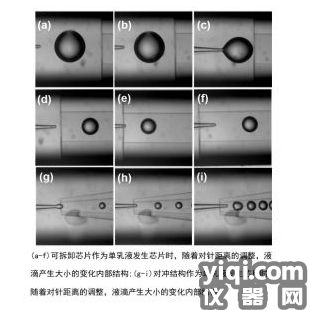 可拆卸双重乳液滴毛细管玻璃芯片
可拆卸双重乳液滴毛细管玻璃芯片
报价:面议 已咨询 93次
 微流体3D紧凑型定位系统rotAXYS
微流体3D紧凑型定位系统rotAXYS
报价:面议 已咨询 1127次
 微流体高压注射泵Fusion6000
微流体高压注射泵Fusion6000
报价:¥47500 已咨询 1761次
 独立双通道注射泵Fusion4000
独立双通道注射泵Fusion4000
报价:¥35500 已咨询 1409次
 微流体除泡器-去除管路液体中的气泡
微流体除泡器-去除管路液体中的气泡
报价:面议 已咨询 2146次
 微流体微流控PDMS膜加工套装
微流体微流控PDMS膜加工套装
报价:面议 已咨询 981次
 倒置生物显微镜AE31E
倒置生物显微镜AE31E
报价:面议 已咨询 2707次
 氟油40(Fluo-Oil 40)
氟油40(Fluo-Oil 40)
报价:面议 已咨询 460次








①本文由仪器网入驻的作者或注册的会员撰写并发布,观点仅代表作者本人,不代表仪器网立场。若内容侵犯到您的合法权益,请及时告诉,我们立即通知作者,并马上删除。
②凡本网注明"来源:仪器网"的所有作品,版权均属于仪器网,转载时须经本网同意,并请注明仪器网(www.yiqi.com)。
③本网转载并注明来源的作品,目的在于传递更多信息,并不代表本网赞同其观点或证实其内容的真实性,不承担此类作品侵权行为的直接责任及连带责任。其他媒体、网站或个人从本网转载时,必须保留本网注明的作品来源,并自负版权等法律责任。
④若本站内容侵犯到您的合法权益,请及时告诉,我们马上修改或删除。邮箱:hezou_yiqi
参与评论
登录后参与评论