一、引言
癌症,作为严重威胁人类健康的重大疾病,其治疗一直是医学领域研究的焦点。传统的kA治疗手段,如手术、放疗和化疗,虽在一定程度上取得了成效,但存在诸多局限性,如化疗药物的毒副作用、肿瘤细胞的多药耐药性等。寻找高效、低毒且具有靶向性的kA治疗策略迫在眉睫。外泌体,作为一种新型的纳米级细胞外囊泡,因其独特的生物学特性,近年来逐渐成为kA治疗中极具潜力的药物载体,为癌症治疗带来了新的希望。
二、外泌体的生物学特性
外泌体直径通常在30 - 150纳米之间,广泛存在于各种生物体液中,如血液、尿液、唾液等。它们由细胞内的多囊泡体与细胞膜融合后释放到细胞外环境。外泌体的膜结构与来源细胞的细胞膜相似,这使得它们在体内具有良好的生物相容性和低免疫原性。同时,外泌体内部包裹着多种生物活性分子,包括蛋白质、核酸(如mRNA、miRNA)和脂质等,这些成分不仅反映了来源细胞的生理病理状态,还能在细胞间通讯中发挥重要作用,为其作为药物载体奠定了基础。
2025 年 1 月 29 日,瑞士伯尔尼大学等团队在行业期刊Cells上发表了题为Mesenchymal Stem-Cell-Derived Exosomes as Novel Drug Carriers in Anti-Cancer Treatment: A Myth or Reality?(间充质干细胞衍生的外泌体作为kA治疗的新型药物载体:神话还是现实?)的综述报告。在这篇综述文章中,研究人员总结了 MSCs-Exos 在kA治疗中的治疗潜力的当前知识和未来前景,为恶性疾病的靶向治疗开辟了新途径。

三、外泌体作为kA药物载体的优势
(一)天然的靶向性
外泌体具有天然的靶向特定细胞或组织的能力。肿瘤细胞来源的外泌体可以优先归巢到肿瘤微环境中的细胞,包括肿瘤细胞本身、肿瘤相关成纤维细胞和免疫细胞等。这一特性源于外泌体表面存在的一些特异性蛋白,如整合素等,它们能够与靶细胞表面的相应受体结合,实现精准“投递”。例如,某些肿瘤来源的外泌体表面的整合素可特异性识别肿瘤血管内皮细胞表面的配体,使外泌体更容易聚集在肿瘤组织部位,提高kA药物在肿瘤局部的浓度,增强治疗效果。
(二)良好的生物相容性和低免疫原性
外泌体来源于细胞自身,其膜结构和组成成分与宿主细胞相似,因此在体内具有良好的生物相容性,不易引起免疫反应。与传统的合成纳米载体相比,外泌体不会被免疫系统迅速识别和清除,能够在血液循环中保持相对稳定,延长药物的作用时间。这使得外泌体作为药物载体可以更有效地将药物输送到靶部位,减少因载体引发的不良反应,提高患者的耐受性。
(三)跨越生物屏障的能力
人体存在多种生物屏障,如血脑屏障、胎盘屏障等,这给kA药物的递送带来了巨大挑战。外泌体由于其纳米级的尺寸和特殊的膜结构,具有跨越生物屏障的能力。研究表明,外泌体可以通过与内皮细胞相互作用,以胞吞或受体介导的方式穿越血脑屏障,将携带的药物递送至脑部肿瘤细胞。这种跨越生物屏障的特性为脑部肿瘤等难治性癌症的治疗提供了新的途径。
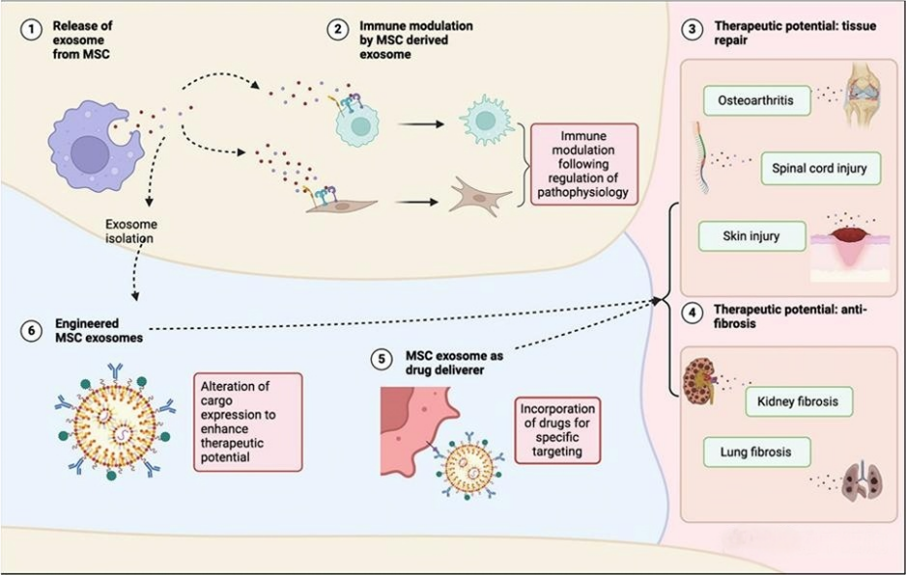
四、外泌体负载kA药物的策略
(一)直接共孵育法
将外泌体与kA药物直接混合孵育是一种简单且常用的方法。在适当的条件下,药物可以通过被动扩散或主动运输的方式进入外泌体内部。例如,一些亲脂性药物能够自发地插入外泌体的脂质双层膜中;而对于亲水性药物,可以利用外泌体膜上的转运蛋白或通道,在能量依赖或非依赖的情况下将药物摄取到外泌体内部。这种方法操作简便,但药物负载效率可能较低,且难以控制药物在外泌体中的分布和释放。
(二)电穿孔法
电穿孔法是通过施加短暂的高电场脉冲,使外泌体膜瞬间形成纳米级的孔道,从而促使药物进入外泌体内部。该方法能够显著提高药物的负载效率,适用于多种类型的kA药物,包括核酸类药物。然而,电穿孔过程可能会对外泌体的结构和功能造成一定的损伤,影响其在体内的稳定性和生物学活性。因此,需要优化电穿孔参数,以在保证药物负载效率的同时,尽量减少对外泌体的不良影响。
(三)超声法
超声法利用超声波的空化效应,在溶液中产生微小的气泡,气泡破裂时产生的局部高温、高压以及强烈的剪切力可以促使外泌体膜形成瞬时孔隙,进而将药物载入外泌体。与电穿孔法相比,超声法相对温和,对外泌体的损伤较小。但超声的强度、时间和频率等参数需要精确控制,以确保药物负载的效果和外泌体的完整性。
五、外泌体在kA治疗中的应用现状
(一)化疗药物递送
将化疗药物包裹于外泌体中,可以改善药物的药代动力学特性,降低其全身毒性。例如,阿霉素是一种常用的化疗药物,但它对心脏等正常组织具有严重的毒副作用。研究人员将阿霉素负载到外泌体中,发现外泌体能够有效地将阿霉素递送至肿瘤细胞,提高肿瘤组织内药物浓度的同时,减少了药物在心脏等正常组织中的分布,从而降低了心脏毒性,增强了kA疗效。
(二)基因治疗载体
外泌体作为基因治疗载体具有独特的优势。它们可以包裹核酸类药物,如siRNA、miRNA和mRNA等,保护这些核酸免受核酸酶的降解,并将其递送至靶细胞。通过外泌体递送的siRNA能够特异性地沉默肿瘤相关基因的表达,抑制肿瘤细胞的增殖、迁移和侵袭。例如,针对某些致癌基因设计的siRNA,经外泌体递送至肿瘤细胞后,可以有效地降低该基因的表达水平,诱导肿瘤细胞凋亡。
(三)免疫治疗佐剂
外泌体在免疫调节方面也发挥着重要作用,可作为免疫治疗的佐剂。肿瘤来源的外泌体可以携带肿瘤相关抗原,激活机体的免疫系统,增强免疫细胞对肿瘤细胞的识别和杀伤能力。同时,外泌体还可以调节肿瘤微环境中的免疫抑制状态,促进免疫细胞向肿瘤部位浸润,协同免疫检查点抑制剂等免疫治疗药物,提高kA免疫治疗的效果。
六、挑战与展望
尽管外泌体作为kA治疗的新型药物载体展现出巨大的潜力,但在临床应用中仍面临诸多挑战。首先,外泌体的大规模制备和纯化技术有待进一步优化,以满足临床治疗所需的数量和质量要求。目前,外泌体的分离方法主要包括超速离心、密度梯度离心、免疫亲和捕获等,这些方法普遍存在操作繁琐、耗时较长、产量低以及纯度不高等问题。其次,外泌体在体内的作用机制尚未完全明确,例如外泌体与靶细胞的相互作用方式、药物释放机制等,深入了解这些机制对于优化外泌体药物载体系统至关重要。此外,外泌体作为药物载体的安全性评估也需要更加全面和深入的研究,包括长期毒性、潜在的免疫反应以及对正常生理功能的影响等。
展望未来,随着生物技术和纳米技术的不断发展,相信这些挑战将逐步得到解决。外泌体有望成为癌症精准治疗的重要工具,与其他治疗手段相结合,为癌症患者带来更好的治疗效果和生存质量。通过多学科交叉研究,深入挖掘外泌体的生物学特性和功能,优化其作为药物载体的性能,必将推动外泌体在kA治疗领域的广泛应用,开启癌症治疗的新篇章。
埃泽思生物公司
埃泽思生物( Applied Cell)总部位于上海,专注于细胞治疗、再生医学等相关领域上游产品的研发与生产,公司产品在细胞与基因治疗、细胞样本存储,药物发现,科学研究等领域有广泛应用。

埃泽思生物MSC产品推荐
人间充质干细胞成骨分化试剂盒AC-1001027
人间充质干细胞成软骨分化试剂盒AC-1001028
人间充质干细胞成脂分化试剂盒AC-1001029


全部评论(0条)
 AC-1001027人间充质干细胞成骨分化试剂盒,埃泽思生物,染色效果好,着色清晰
AC-1001027人间充质干细胞成骨分化试剂盒,埃泽思生物,染色效果好,着色清晰
报价:¥1976 已咨询 75次
 无血清细胞冻存液(治.疗级)无糖(埃泽思生物)
无血清细胞冻存液(治.疗级)无糖(埃泽思生物)
报价:¥1330 已咨询 1601次
 人脐带间充质干细胞无血清培养基(无酚红)
人脐带间充质干细胞无血清培养基(无酚红)
报价:¥1588 已咨询 1552次
 成骨检测染
成骨检测染
报价:¥358 已咨询 1715次
 人间充质干细胞成骨分化试剂盒
人间充质干细胞成骨分化试剂盒
报价:¥1976 已咨询 908次
 人多能干细胞培养基
人多能干细胞培养基
报价:¥2066 已咨询 1081次
 埃泽思人类多能干细胞完全培养基AC-1001001
埃泽思人类多能干细胞完全培养基AC-1001001
报价:¥2526 已咨询 804次
 Xeno-Free细胞消化液 埃泽思生物AC-1001024/1001025
Xeno-Free细胞消化液 埃泽思生物AC-1001024/1001025
报价:¥260 已咨询 621次
2024-08-16
2023-04-11
 埃泽思生物AppliedCell®|无动物源成分的冻存液,为何越来越受青睐?
埃泽思生物AppliedCell®|无动物源成分的冻存液,为何越来越受青睐?
2026-01-07
2024-10-15
2024-11-22
2024-11-29









①本文由仪器网入驻的作者或注册的会员撰写并发布,观点仅代表作者本人,不代表仪器网立场。若内容侵犯到您的合法权益,请及时告诉,我们立即通知作者,并马上删除。
②凡本网注明"来源:仪器网"的所有作品,版权均属于仪器网,转载时须经本网同意,并请注明仪器网(www.yiqi.com)。
③本网转载并注明来源的作品,目的在于传递更多信息,并不代表本网赞同其观点或证实其内容的真实性,不承担此类作品侵权行为的直接责任及连带责任。其他媒体、网站或个人从本网转载时,必须保留本网注明的作品来源,并自负版权等法律责任。
④若本站内容侵犯到您的合法权益,请及时告诉,我们马上修改或删除。邮箱:hezou_yiqi
 飞秒激光打造“防冰盔甲”,超疏水表面光热防冰 又强又稳”
飞秒激光打造“防冰盔甲”,超疏水表面光热防冰 又强又稳”
参与评论
登录后参与评论